
OK, also – was ist ein Atom und was hat es mit Molekülen zu tun?
Lassen Sie uns klein reden, und ich meine wirklich klitzeklein. ATOME sind die Grundbausteine von allem, was Sie um sich herum sehen können, und sogar von vielen Dingen, die Sie nicht sehen können, wie die Luft, die Sie atmen. Atome sind so klein, dass es Millionen und Milliarden und Billionen in dem kleinsten Fleck gibt, den Sie sehen können. Feststoffe, Flüssigkeiten, Gase – alle Materie – bestehen aus Atomen (oder anderen Dingen, wie Molekülen, die aus Atomen gemacht sind)!
 ELEMENTE sind die Arten von Atomen, die wir haben können. Kohlenstoff ist ein Element, Wasserstoff ist ein Element, und auch Sauerstoff ist ein Element. (Wir können sie mit ihren Namen oder mit ihren Symbolen benennen – C für Kohlenstoff, H für Wasserstoff und O für Sauerstoff). Alle Elemente sind in einem Periodensystem aufgelistet. Wenn es in der Tabelle steht, ist es ein Element!
ELEMENTE sind die Arten von Atomen, die wir haben können. Kohlenstoff ist ein Element, Wasserstoff ist ein Element, und auch Sauerstoff ist ein Element. (Wir können sie mit ihren Namen oder mit ihren Symbolen benennen – C für Kohlenstoff, H für Wasserstoff und O für Sauerstoff). Alle Elemente sind in einem Periodensystem aufgelistet. Wenn es in der Tabelle steht, ist es ein Element!
Atome können sich zusammenschließen – sie bilden Bindungen miteinander – um MOLEKULE zu bilden. Zum Beispiel haken sich zwei Wasserstoffatome zusammen, um ein Wasserstoffmolekül zu bilden, kurz H2. Ziemlich einfach, nicht wahr?
Zum Beispiel haken sich zwei Wasserstoffatome zusammen, um ein Wasserstoffmolekül zu bilden, kurz H2. Ziemlich einfach, nicht wahr?
Klicken Sie hier, um sich ein 3-D-Modell von Wasserstoff (H2) anzusehen.
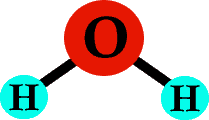
Wenn Sie nun ein Sauerstoffatom zwischen diese beiden Wasserstoffatome setzen, haben Sie ein Wassermolekül – H2O!
Klicken Sie hier, um Wasser (H2O) in 3-D zu sehen.
Jeder Atomtyp bildet typischerweise die gleiche Anzahl von Bindungen (sie neigen dazu, auf diese Weise stur zu sein). Ein Wasserstoffatom bildet zum Beispiel eine Bindung, ein Sauerstoffatom zwei, und Kohlenstoff bildet vier Bindungen. Schauen Sie sich das Wassermolekül noch einmal an – jeder Wasserstoff hat eine Bindung, und der Sauerstoff in der Mitte hat zwei Bindungen.
Moleküle können viel größer sein. Ein Molekül Vitamin C besteht aus 20 Atomen (6 Kohlenstoffe, 8 Wasserstoffatome und 6 Sauerstoffatome – das ist C6H8O6). Wenn Sie diese 20 Atome von Vitamin C nehmen und sie in einer anderen Reihenfolge miteinander verbinden, erhalten Sie ein völlig anderes Molekül, das nicht nur anders aussieht, sondern auch anders wirkt. (Wenn deine Beine aus deinem Kopf ragen würden, würdest du dich auch komisch verhalten!)
| Vitamin C C6H8O6 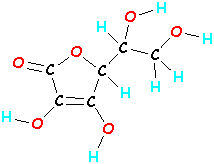 |
Sonstiges C6H8O6 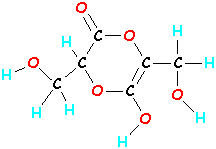 |
So, Moleküle sind Atome, die aneinander gebunden sind, aber nicht auf irgendeine Weise. Wenn man ändert, welches Atom an welches gebunden ist, kann man die Eigenschaften eines Moleküls ändern, das heißt, wie es aussieht und sich verhält – und das ändert, wie ein ganzer Haufen von Molekülen, die zusammenhängen, aussehen und sich verhalten. Zum Beispiel ist Wasser eine Flüssigkeit, Wasserstoff ist ein Gas, und Vitamin C ist ein Feststoff.
„SO WAS?!!“, fragen Sie. Nun, wenn wir über Polymere sprechen, kann die Art und Weise, wie die Atome aneinander gebunden sind, einen RIESIGEN Einfluss darauf haben, wie sich etwas, das aus diesen Polymeren besteht, anfühlt und reagiert, wenn man darauf schlägt oder tritt oder es gegen die Wand wirft. Bleibt es an der Wand kleben oder prallt es ab?
Eine Bindungserfahrung
Die Art der Bindung, über die wir hier gesprochen haben, nennt man „kovalente Bindung“, was bedeutet, dass sie durch den Austausch von Elektronen zwischen zwei Atomen entsteht.
Mehr über Bindungen und die Struktur der Atome hier, ansonsten ….
Let’s talk POLYMERS !!!
 |
Zurück zu den Polymer-Grundlagen |
 |
Zurück zur Hauptseite |