Alle Salze und Ionen, die sich im Meerwasser lösen, tragen zu dessen Gesamtsalzgehalt bei. Der Salzgehalt des Meerwassers wird normalerweise als Gramm Salz pro Kilogramm (1000 g) Meerwasser angegeben. Im Durchschnitt sind etwa 35 g Salz in jedem 1 kg Meerwasser vorhanden, so dass wir sagen, dass der durchschnittliche Salzgehalt des Ozeans 35 Teile pro Tausend (ppt) beträgt. Beachten Sie, dass 35 ppt 3,5 % (Teile pro Hundert) entsprechen. Einige Quellen verwenden nun praktische Salinitätseinheiten (PSU), um die Salinitätswerte auszudrücken, wobei 1 PSU = 1 ppt. Die Einheiten werden nicht mit angegeben, so dass wir uns einfach auf einen Salzgehalt von 35 beziehen können.
Im Meer sind viele verschiedene Stoffe gelöst, aber sechs Ionen machen etwa 99,4 % aller gelösten Ionen im Meerwasser aus. Diese sechs Hauptionen sind (Tabelle 5.3.1):
Tabelle 5.3.1 Die sechs Hauptionen im Meerwasser
| g/kg in Meerwasser | Gewichts-% der Ionen | |
|---|---|---|
| Chlorid Cl- | 19.35 | 55,07% | Natrium Na+ | 10,76 | 30,6% |
| Sulfat SO42- | 2,71 | 7.72% |
| Magnesium Mg2+ | 1.29 | 3.68% |
| Kalzium Ca2+ | 0.41 | 1.17% |
| Kalium K+ | 0.39 | 1.1% |
| 99,36% |

Chlorid und Natrium, die Bestandteile von Kochsalz (Natriumchlorid NaCl), machen über 85% der Ionen im Meer aus, weshalb Meerwasser salzig schmeckt (Abbildung 5.3.1). Zusätzlich zu den Hauptbestandteilen gibt es zahlreiche Nebenbestandteile; Radionukleotide, organische Verbindungen, Metalle usw. Diese Nebenbestandteile sind in Konzentrationen von ppm (parts per million) oder ppb (parts per billion) zu finden, im Gegensatz zu den Hauptbestandteilen, die weitaus häufiger vorkommen (ppt) (Tabelle 5.3.2). Zum Vergleich: 1 ppm = 1 mg/kg oder das Äquivalent von 1 Teelöffel Zucker, der in 14.000 Dosen Soda gelöst ist. 1 ppb = 1 μg/kg oder das Äquivalent von 1 Teelöffel einer Substanz, die in fünf Schwimmbecken von olympischer Größe gelöst ist! Diese Nebenbestandteile stellen zahlreiche Substanzen dar, machen aber zusammen weniger als 1 % der Ionen im Meerwasser aus. Einige von ihnen mögen als Mineralien und Spurenelemente wichtig sein, die für lebende Organismen lebenswichtig sind, aber sie haben keinen großen Einfluss auf den Gesamtsalzgehalt. Aber angesichts der enormen Größe der Ozeane können selbst Materialien, die in Spuren vorkommen, ziemlich große Reserven darstellen. Zum Beispiel ist Gold ein Spurenelement im Meerwasser, das in Konzentrationen von Teilen pro Billion zu finden ist, doch wenn man das gesamte Gold in nur einem km3 Meerwasser extrahieren könnte, wäre es etwa 20 Millionen Dollar wert!
Tabelle 5.3.2 Konzentrationen einiger weniger Elemente im Meerwasser
| g/kg in Meerwasser | g/kg in Meerwasser | ||
|---|---|---|---|
| Carbon | 0.028 | Eisen | 2 x 10-6 |
| Stickstoff | 0.0115 | Mangan | 2 x 10-7 |
| Sauerstoff | 0.006 | Kupfer | 1 x 10-7 |
| Silizium | 0.002 | Quecksilber | 3 x 10-8 |
| Phosphor | 6 x 10-5 | Gold | 4 x 10-9 |
| Uran | 3.2 x 10-6 | Blei | 5 x 10-10 |
| Aluminium | 2 x 10-6 | Radon | 6 x 10-.19 |
Da die sechs Hauptionen im Meerwasser über 99 % des gesamten Salzgehaltes ausmachen, haben Änderungen in der Häufigkeit der Nebenbestandteile wenig Einfluss auf den Gesamtsalzgehalt. Darüber hinaus besagt die Regel der konstanten Proportionen, dass, obwohl der absolute Salzgehalt des Meerwassers an verschiedenen Orten unterschiedlich sein kann, die relativen Proportionen der sechs Hauptionen in diesem Wasser immer konstant sind. Unabhängig vom Gesamtsalzgehalt einer Meerwasserprobe entfallen beispielsweise 55% des Gesamtsalzgehalts auf Chlorid, 30% auf Natrium und so weiter. Da sich der Anteil dieser Hauptionen nicht ändert, nennen wir sie konservative Ionen.
Bei diesen konstanten Anteilen kann man zur Berechnung des Gesamtsalzgehalts einfach die Konzentration nur eines der Hauptionen messen und diesen Wert zur Berechnung des Rests verwenden. Traditionell ist Chlorid das gemessene Ion, weil es am häufigsten vorkommt und daher am einfachsten genau zu messen ist. Multipliziert man die Chloridkonzentration mit 1,8, erhält man den Gesamtsalzgehalt. Ein Beispiel: Abbildung 5.3.1: 19,25 g/kg (ppt) Chlorid x 1,8 = 35 ppt. Für schnelle Messungen des Salzgehalts wird heute oft die elektrische Leitfähigkeit anstelle der Bestimmung der Chloridkonzentration verwendet (siehe Kasten unten).
Es gibt eine Reihe von Methoden zur Messung des Salzgehalts von Wasser. Die präzisesten Messungen nutzen die direkte chemische Analyse des Meerwassers in einer Laborumgebung, aber es gibt eine Reihe von Möglichkeiten, den Salzgehalt direkt im Feld zu messen. Für eine schnelle Abschätzung des Salzgehalts kann ein tragbares Refraktometer verwendet werden (rechts).

Dieses Instrument misst den Grad der Beugung oder Brechung von Lichtstrahlen beim Durchgang durch eine Flüssigkeit. Je größer der Anteil an gelösten Salzen in der Probe ist, desto größer ist der Grad der Lichtbrechung. Der Beobachter fängt einen Wassertropfen auf dem blauen Schirm ein und blickt durch das Okular. An der Trennlinie zwischen dem blauen und dem weißen Teil der Skala (Einschub) kann der Salzgehalt abgelesen werden.
Für genauere Messungen verwenden die meisten Ozeanographen ein Gerät, das die elektrische Leitfähigkeit misst. Ein elektrischer Strom wird zwischen zwei in Wasser getauchten Elektroden geleitet, und je höher der Salzgehalt ist, desto leichter wird der Strom geleitet (die Ionen im Meerwasser leiten elektrische Ströme). Leitfähigkeitssonden werden oft in einem Instrument gebündelt, das CTD genannt wird, was für Conductivity (Leitfähigkeit), Temperature (Temperatur) und Depth (Tiefe) steht, die am häufigsten gemessenen Parameter. Moderne CTDs können mit einer Reihe von Sonden ausgestattet sein, die Parameter wie Licht, Trübung (Wasserklarheit), gelöste Gase usw. messen. CTDs können große Instrumente sein (unten), aber auch kleine handgehaltene Salzgehaltssonden sind weit verbreitet.

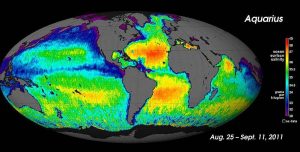
Für großflächige Salzgehaltsmessungen können Ozeanographen Satelliten einsetzen, wie zum Beispiel den Aquarius-Satelliten, der in der Lage war, Salzgehaltsunterschiede an der Oberfläche von nur 0,2 PSU zu messen, während er die Meeresoberfläche alle sieben Tage kartierte (unten).
Es ist wichtig, sich bewusst zu machen, dass die Regel der konstanten Proportionen zwar für den größten Teil des Ozeans gilt, es aber bestimmte Küstengebiete geben kann, in denen viele Flusseinleitungen diese Proportionen leicht verändern können. Außerdem ist es wichtig, sich daran zu erinnern, dass die Regel der konstanten Proportionen nur für die Hauptionen gilt. Die Anteile der Nebenionen können schwanken, aber bedenken Sie, dass sie einen sehr geringen Beitrag zum Gesamtsalzgehalt leisten. Da die Konzentrationen der Nebenionen nicht konstant sind, werden diese als nicht-konservative Ionen bezeichnet.
Warum sind die Hauptionen in konstanten Anteilen vorhanden? Es gibt einen konstanten Eintrag von Ionen aus Flussabflüssen und anderen Prozessen, normalerweise in sehr unterschiedlichen Verhältnissen zu dem, was man im Ozean findet. Warum ändern sich also die Verhältnisse in den Ozeanen nicht? Die meisten Ionen, die von Flüssen abgeleitet werden, haben im Vergleich zu Ionen im Meerwasser recht geringe Verweilzeiten (siehe Abschnitt 5.2), da sie normalerweise in biologischen Prozessen verwendet werden. Diese geringen Verweilzeiten erlauben es den Ionen nicht, sich zu akkumulieren und den Salzgehalt zu verändern. Außerdem beträgt die Durchmischungszeit des Weltozeans etwa 1000 Jahre, was im Vergleich zu den Verweilzeiten der Hauptionen, die mehrere zehn Millionen Jahre lang sein können, sehr kurz ist. Während der Verweilzeit eines einzelnen Ions hat sich der Ozean also zahlreiche Male gemischt, und die Hauptionen haben sich gleichmäßig im Ozean verteilt.
Variationen im Salzgehalt
Der Gesamtsalzgehalt im offenen Ozean beträgt im Durchschnitt 33-37 ppt, kann aber an verschiedenen Orten stark variieren. Da aber die Hauptionenanteile konstant sind, müssen die regionalen Salzgehaltsunterschiede eher auf den Wassereintrag und -entzug als auf die Zugabe oder den Entzug von Ionen zurückzuführen sein. Die Zufuhr von Süßwasser erfolgt durch Prozesse wie Niederschlag, Abfluss vom Land und schmelzendes Eis. Der Süßwasserentzug erfolgt in erster Linie durch Verdunstung und Gefrieren (wenn Meerwasser gefriert, besteht das entstehende Eis größtenteils aus Süßwasser und die Salze werden ausgeschlossen, wodurch das verbleibende Wasser noch salziger wird). Daher spielen Unterschiede in den Raten von Niederschlag, Verdunstung, Flussabfluss und Eisbildung eine wichtige Rolle bei regionalen Schwankungen des Salzgehalts. Die Ostsee zum Beispiel hat einen sehr niedrigen Oberflächensalzgehalt von etwa 10 ppt, weil sie ein größtenteils geschlossenes Gewässer mit viel Flusszufluss ist. Im Gegensatz dazu ist das Rote Meer sehr salzhaltig (ca. 40 ppt), was auf den Mangel an Niederschlägen und die heiße Umgebung zurückzuführen ist, die zu einer hohen Verdunstung führt.
Eines der salzhaltigsten großen Gewässer der Erde ist das Tote Meer zwischen Israel und Jordanien. Der Salzgehalt im Toten Meer liegt bei etwa 330 ppt und ist damit fast zehnmal salziger als der des Ozeans. Dieser extrem hohe Salzgehalt ist eine Folge der heißen, trockenen Bedingungen im Nahen Osten, die zu hohen Verdunstungsraten führen. Außerdem wurde in den 1950er Jahren der Abfluss des Jordan vom Toten Meer weggeleitet, so dass es keinen signifikanten Süßwassereintrag mehr gibt. Ohne Zufluss und mit hoher Verdunstung sinkt der Wasserspiegel des Toten Meeres mit einer Rate von etwa 1 m pro Jahr. Der hohe Salzgehalt macht das Wasser sehr dicht, was Auftriebskräfte erzeugt, die es Menschen ermöglichen, leicht an der Oberfläche zu schwimmen. Aber der hohe Salzgehalt bedeutet auch, dass das Wasser für die meisten lebenden Organismen zu salzig ist, so dass nur Mikroben in der Lage sind, es ihr Zuhause zu nennen; daher der Name Totes Meer. Aber so salzig das Tote Meer auch sein mag, es ist nicht das salzigste Gewässer der Erde. Diese Auszeichnung gehört derzeit dem Gaet’ale Pond in Äthiopien, mit einem Salzgehalt von 433 ppt!
Latitudinale Variationen
Während die lokalen Bedingungen wichtig sind, um die Salzgehaltsmuster an jedem einzelnen Ort zu bestimmen, gibt es einige globale Muster, die weitere Untersuchungen erfordern. Die Temperatur ist am Äquator am höchsten und in der Nähe der Pole am niedrigsten, so dass man in äquatorialen Regionen höhere Verdunstungsraten und damit einen höheren Salzgehalt erwarten würde (Abbildung 5.3.2). Dies ist im Allgemeinen der Fall, aber in der Abbildung unten scheint der Salzgehalt direkt am Äquator etwas niedriger zu sein als in etwas höheren Breitengraden. Das liegt daran, dass in äquatorialen Regionen auch regelmäßig viel Regen fällt, der das Oberflächenwasser entlang des Äquators verdünnt. Die höheren Salzgehalte finden sich also in subtropischen, warmen Breiten mit hoher Verdunstung und weniger Niederschlag. An den Polen gibt es wenig Verdunstung, was in Verbindung mit der Eis- und Schneeschmelze zu einem relativ niedrigen Oberflächensalzgehalt führt. Das Bild unten zeigt den hohen Salzgehalt im Mittelmeer; dieses befindet sich in einer warmen Region mit hoher Verdunstung, und das Meer ist weitgehend von der Vermischung mit dem restlichen Wasser des Nordatlantiks isoliert, was zu einem hohen Salzgehalt führt. Niedrigere Salzgehalte, wie z.B. um Südostasien, sind das Ergebnis von Niederschlägen und hohen Flusseinträgen.

Abbildung 5.3.3 zeigt die mittleren globalen Unterschiede zwischen Verdunstung und Niederschlag (Verdunstung – Niederschlag). Grüne Farben stellen Gebiete dar, in denen der Niederschlag die Verdunstung übersteigt, während braune Regionen diejenigen sind, in denen die Verdunstung größer ist als die Niederschläge. Beachten Sie die Korrelation zwischen Niederschlag, Verdunstung und Oberflächensalzgehalt wie in Abbildung 5.3.2.

Vertikale Variation
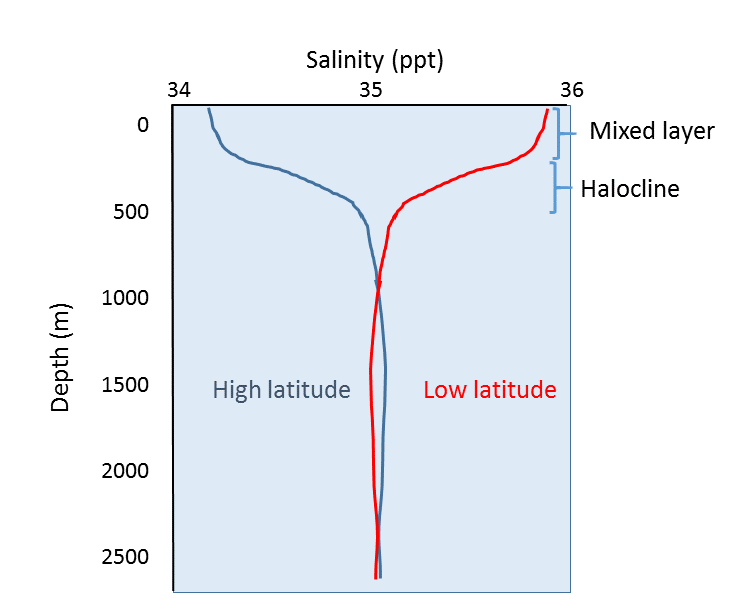
Zusätzlich zur geographischen Variation des Salzgehalts gibt es auch Veränderungen des Salzgehalts mit der Tiefe. Wie wir gesehen haben, sind die meisten Unterschiede im Salzgehalt auf Schwankungen der Verdunstung, des Niederschlags, des Abflusses und der Eisbedeckung zurückzuführen. Alle diese Prozesse finden an der Meeresoberfläche und nicht in der Tiefe statt, so dass die ausgeprägtesten Unterschiede im Salzgehalt im Oberflächenwasser zu finden sein sollten. Der Salzgehalt in tieferem Wasser bleibt relativ einheitlich, da er von diesen Oberflächenprozessen nicht beeinflusst wird. Einige repräsentative Salinitätsprofile sind in Abbildung 5.3.4 dargestellt. An der Oberfläche weisen die obersten etwa 200 m einen relativ einheitlichen Salzgehalt in der sogenannten Mischschicht auf. Winde, Wellen und Oberflächenströmungen wirbeln das Oberflächenwasser auf, was zu einer starken Durchmischung in dieser Schicht und relativ gleichmäßigen Salzgehaltsbedingungen führt. Unterhalb der Mischschicht befindet sich ein Bereich, in dem sich der Salzgehalt über eine geringe Tiefenänderung schnell ändert. Diese Zone der schnellen Veränderung wird Halokline genannt und stellt einen Übergang zwischen der Mischschicht und dem tiefen Ozean dar. Unterhalb der Halokline kann der Salzgehalt bis zum Meeresboden nur geringe Schwankungen aufweisen, da diese Region weit von den Oberflächenprozessen entfernt ist, die den Salzgehalt beeinflussen. In der Abbildung unten ist der niedrige Oberflächensalzgehalt in hohen Breitengraden und der höhere Oberflächensalzgehalt in niedrigen Breitengraden zu sehen. Doch trotz der Oberflächenunterschiede kann der Salzgehalt in der Tiefe an beiden Orten sehr ähnlich sein.
Ein Atom oder Molekül, das entweder Elektronen gewonnen oder verloren hat und somit geladen wurde (5.1)
die Konzentration von gelösten Ionen in Wasser (5.3)
ein einheitsloses Maß für den Salzgehalt, das Teilen pro Tausend entspricht (5.3)
die sechs Ionen, die über 99 % der Ionen im Ozean ausmachen (Chlorid, Natrium, Sulfat, Magnesium, Kalzium, Kalium) (5.3)
die Hauptionen im Meerwasser sind immer in den gleichen Anteilen vorhanden, unabhängig vom Gesamtsalzgehalt (5.3)
Ionen, deren Anteile unabhängig vom Gesamtsalzgehalt gleich sind; die Hauptionen im Meerwasser (5.3)
Ionen im Meerwasser, deren Anteile bei Änderungen des Salzgehaltes schwanken (5.3)
Fluss von Wasser ein Gefälle hinunter, entweder über die Bodenoberfläche oder innerhalb einer Reihe von Kanälen (12.2)
die durchschnittliche Zeitspanne, die ein Element im Ozean verbleibt, bevor es entfernt wird (5.2)
Promille
die Entfernung nördlich oder südlich des Äquators, gemessen als Winkel vom Äquator (2.1)
die oberste Schicht des Ozeans, in der Winde, Wellen und Strömungen das Wasser vermischen, so dass die Bedingungen relativ konstant sind; etwa die obersten 100 m (5.3)
wo es eine dramatische Änderung des Salzgehalts über eine kleine Änderung der Tiefe gibt (5.3)