Der Mechanismus, mit dem die Wohl-Ziegler-Reaktion abläuft, wurde 1953 von Paul Goldfinger vorgeschlagen, und sein Reaktionsmechanismus ist einer von zwei vorgeschlagenen Wegen, über die die aliphatische, allylische und benzylische Bromierung mit N-Bromsuccinimid (NBS) erfolgt. Es hat sich gezeigt, dass der Goldfinger-Mechanismus der richtige Mechanismus ist, im Gegensatz zu dem zuvor akzeptierten Mechanismus, der von George Bloomfield vorgeschlagen wurde, der sich, obwohl er bei Selektivitätsstudien konsistent war, als zu vereinfachend herausstellte.
Die Erzeugung von NBS-Radikalen, die im Bloomfield-Mechanismus dargestellt wird, hat sich als weitaus schwieriger erwiesen, als man es sich vorgestellt hatte, als er vorgeschlagen wurde, weshalb er im Laufe der Jahre als richtiges Modell versagt hat; es gibt jedoch Hinweise darauf, dass der Bloomfield-Mechanismus für die Oxidation von Alkoholen mit NBS noch akzeptabel ist. Im Goldfinger-Mechanismus besteht der Zweck der NBS einfach darin, eine sehr niedrige Konzentration von molekularem Brom aufrechtzuerhalten, während im Bloomfield-Mechanismus ihr Zweck die Erzeugung des anfänglichen Radikals ist, das in der Reaktion verwendet wird, was wiederum ein ziemlich schwieriger Prozess sein kann. Dies liegt daran, dass es eine besondere Berücksichtigung für das Verhalten des NBS-Radikals erfordert; der einzige Weg, wie es möglicherweise funktionieren kann, wie in Bloomfields Mechanismus vorgeschlagen, ist, wenn die Dissoziationsenergie für die N-Br-Bindung in NBS kleiner ist als die für Br2, und es gibt viele Hinweise, die auf ein gegenteiliges Verhalten hindeuten. Goldfingers vorgeschlagener Mechanismus erfordert keine besonderen Überlegungen, da sich alle radikalischen Spezies normal verhalten, und es ist zum Teil deswegen, dass sein Mechanismus als korrekt angesehen wird.

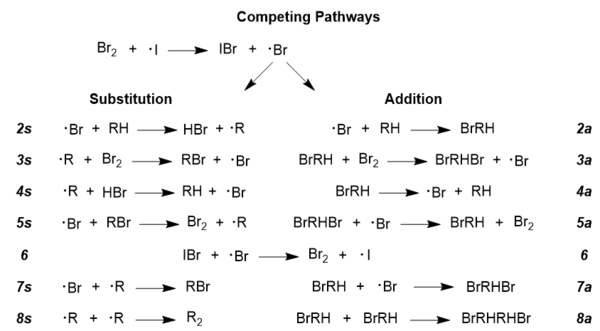
Um den akzeptierten Reaktionsmechanismus weiter zu erforschen, muss man verstehen, dass es bei jeder radikalischen Reaktion konkurrierende Radikalwege gibt; das ist auch in diesem Fall so, da Additions- und Substitutionswege konkurrierend sind. Um das gewünschte bromierte Produkt zu erhalten, muss der Substitutionsweg dominieren, und die Reaktionsbedingungen können tatsächlich so manipuliert werden, dass dieser Weg gegenüber dem weniger wünschenswerten Additionsweg bevorzugt wird. Nachfolgend sind die beiden Wege in ihrer Gesamtheit dargestellt; der Vollständigkeit halber sind in dieser Abbildung auch Nebenreaktionen enthalten, wie z. B. die Schritte 6 und 8; diese Wege sind allgemein für fast alle radikalischen Reaktionen, so dass die NBS hier nicht abgebildet ist, aber ihre Rolle wird weiter unten diskutiert.
Die Rolle von NBS in Goldfingers Mechanismus besteht darin, die Regeneration von molekularem Brom zu fördern, aber einer der zusätzlichen Vorteile der Verwendung von NBS ist, dass es eine niedrige Konzentration von molekularem Brom aufrechterhält, was der Schlüssel zur Förderung der Substitution gegenüber der Addition ist. Es wurden Ratengesetze entwickelt, die das Konkurrenzverhalten dieser Reaktion beschreiben, und sie zeigen eine starke Abhängigkeit von der Konzentration an molekularem Brom; im Folgenden sind die beiden Gleichungen aufgeführt: eine für hohe Bromkonzentrationen und eine für niedrige Bromkonzentrationen.
- Hohe Bromkonzentrationen: r(a/s) = k2a/k2s(1 + k4a/k3a), wobei r(a/s) das Verhältnis von Addition zu Substitution ist und die k-Werte den Konstanten entsprechen, die die oben unter „Konkurrierende Wege“ dargestellten spezifischen Reaktionsschritte beschreiben.
- Niedrige Bromkonzentrationen: r(a/s) = k2ak3a/k2sk4a, wobei die Terme die gleiche Definition wie in der vorherigen Gleichung haben. Es ist zu erkennen, dass in der Gleichung für niedrige Bromkonzentrationen das Verhältnis von Addition zu Substitution direkt proportional zur Konzentration des molekularen Broms ist, so dass eine Senkung der Bromkonzentration den Additionsweg hemmt und einen größeren Grad der Bildung bromierter Produkte fördert.