Acide cinnamique Propriétés chimiques,utilisations,production
Propriétés chimiques
L’acide cinnamique existe sous forme cis et trans. L’isomère le plus stable est l’isomère trans, qui se produit naturellement et est le produit commercial habituel. Il se présente sous forme de prismes monocliniques blancs avec un léger arôme de cannelle. Il est soluble dans l’éthanol, le méthanol, l’éther de pétrole et le chloroforme ; il est facilement soluble dans le benzène, l’éther, l’acétone, l’acide acétique, le disulfure de carbone et les huiles mais insoluble dans l’eau.
L’acide cinnamique a été isolé pour la première fois sous forme de cristaux à partir de l’huile de cannelle par Trommsdorf en 1780. Il pensait qu’il s’agissait d’acide benzoïque. Dumas et Peligot ‘ l’ont identifié en 1835, et en 1856 Bertagnini a réussi à le synthétiser à partir de benzaldéhyde et de chlorure d’acétyle.
L’acide cinnamique subit des réactions typiques d’un groupe carboxyle et d’une double liaison oléfinique. Le groupe carboxyle peut être estérifié pour former des cinnamates, dont certains sont des arômes et des parfums importants. Lorsqu’il est mis en réaction avec des chlorures d’acides inorganiques, tels que le chlorure de thionyle ou les chlorures de phosphore, l’acide cinnamique donne du chlorure de cinnamoyle . Lorsqu’il est chauffé, l’acide cinnamique forme du styrène et du dioxyde de carbone. Avec des agents oxydants ou lorsqu’il est chauffé avec un alcali, la double liaison oléfinique se clive pour donner du benzaldéhyde .
Propriétés physiques et chimiques
L’acide cinnamique, également connu sous le nom d’acétate de benzal, d’acide 3-phényl-2-propénoïque, appartient à une sorte d’acide aromatique insaturé ayant une légère odeur de cannelle. Il se présente dans le baume, l’huile de cannelle et la feuille de coca sous forme libre ou sous forme d’ester. En raison de la présence d’une double liaison, l’acide cinnamique possède deux isomères trans/ cis, la forme cis contenant trois types supplémentaires de polycristaux homogènes. La forme trans et la forme cis existent toutes deux en présence de la nature. La forme trans existe en présence d’huiles essentielles comme le storax, l’huile de cannelle, le baume du Pérou, l’huile de basilic et les feuilles de cacao. La forme cis existe dans l’huile de galanga de Malacca, la forme trans étant plus stable que la forme cis. Les produits disponibles dans le commerce sont principalement sous la forme trans. Sa masse moléculaire relative est de 148,17. La première forme cristalline de la forme cis est appelée acide allocinnamique, le composé précipité dans l’eau étant monoclinique. Il s’agit de cristaux prismatiques incolores à blancs dont la densité relative est de 1,284 (4 ℃), le point de fusion de 42 ℃, le point d’ébullition de 265 ℃ (décomposition ) et 125 ℃ (2,533 × 103Pa) ; il est légèrement soluble dans l’eau (25 ℃ quand 0,937) mais facilement soluble dans l’alcool, l’éther et l’acétate d’éthyle.Le second polymorphe est appelé acide alpha-iso-cinnamique avec le composé précipité à partir de la ligroïne étant le cristal monoclinique. Il se présente sous forme de cristaux prismatiques incolores à blancs dont la mp est de 58 ℃ et le point d’ébullition de 265 ℃. Il est soluble dans l’éthanol, l’acide acétique, le chloroforme et l’acétone et facilement soluble dans l’éther. Le troisième polymorphe est appelé acide bêta-iso-cinnamique ; il se présente sous forme de cristaux prismatiques monocliniques incolores à blancs dont la mp est de 68 ℃. Il est soluble dans l’alcool, l’éther, l’acide acétique, le chloroforme et l’acétone. L’isomère trans précipité à partir d’éthanol dilué appartient au cristal monoclinique et apparaît sous forme de cristaux prismatiques blancs à jaune pâle dont la densité relative est de 1,2475 (4 ℃), le point de fusion de 133 ℃ et le point d’ébullition de 300 ℃. Il est très légèrement soluble dans l’eau (25 ℃ : 0,1 ; 98 ℃ : 0,588), soluble dans l’éthanol (25 ℃ : 23), le chloroforme (15 ℃ : 5,9), facilement soluble dans le benzène, l’éther, l’acétone, l’acide acétique et le disulfure de carbone. Lorsqu’il est distillé à 140 ℃, il subit une décarboxylation pour devenir du styrène (Styrax BP). En cas d’oxydation, il génère de l’acide benzoïque. Les deux isomères cis et trans ont un arôme de miel de fleurs avec une saveur douce et épicée. DL50 orale pour le rat : 2500 mg/kg.
Rôle et objectif
L’acide cinnamique est un type important de matière première organique synthétique. Il est principalement utilisé pour la synthèse du cinnamate de méthyle, du cinnamate d’éthyle et de l’ester benzylique de l’acide cinnamique. Il est largement utilisé dans l’industrie des parfums et l’industrie pharmaceutique. En médecine, il a toujours été utilisé comme insectifuge.
L’acide cinnamique a été utilisé comme épices pour la préparation d’arômes et de saveurs de cerise, d’abricot, de miel et de cannelle ; il peut également être utilisé comme matière première de l’ester d’acide cinnamique. La norme GB2760-1996 de notre pays prévoit que l’acide cinnamique est une épice comestible autorisée ; en outre, il peut également être utilisé comme matière première de la résine photosensible de la série de l’acide polyvinyl cinnamique ; il peut également être utilisé comme matière première pour la synthèse des esters méthylique, éthylique et benzylique. Ces esters, utilisés comme parfums, peuvent être appliqués aux cosmétiques et aux savons, ils peuvent également être utilisés comme anesthésiques locaux, agents hémostatiques et matières premières pharmaceutiques (acide lactique, prénylamine et baclofène, etc.) ; l’acide cinnamique peut également être utilisé comme régulateurs de croissance des plantes et matières premières des pesticides ; agents anticorrosion des fruits et légumes ; matières premières des agents ultraviolets et résine photosensible pour les écrans solaires cosmétiques. L’acide cinnamique peut également être utilisé comme norme pour l’analyse des traces organiques et la détermination de la double liaison, la détermination de la séparation de l’uranium et du vanadium et du thorium.
Utilisations
L’acide cinnamique est un intermédiaire important dans la préparation de ses esters, qui sont utilisés comme parfums, pour les produits pharmaceutiques, et pour la production enzymatique de l-phénylalanine, matière première des édulcorants peptidiques. Le cinnamate de sodium est un inhibiteur de corrosion connu. L’acide cinnamique est également utilisé comme azurant dans les bains galvaniques de zinc sans cyanure, comme inhibiteur de corrosion lors de l’élimination du tartre du zinc et dans les bombes aérosol, comme stabilisateur thermique à faible toxicité pour le poly(chlorure de vinyle) , comme agent de réticulation pour le copolymère téréphtalate de diméthyle – éthylène glycol et les polyuréthanes, comme agent ignifuge pour le polycaprolactame, dans les adhésifs de polyuréthane résistant au lavage pour les fibres de polyester, et pour l’amélioration de la stabilité au stockage des revêtements de résine alkyde modifiés par l’huile de séchage.
Préparation
L’acide cinnamique est également produit par condensation de Knoevenagel du benzaldéhyde avec l’acide malonique en présence de catalyseurs faiblement basiques, tels que l’ammoniac et les amines.
Refluxer ensemble 10ml de benzaldéhyde avec 10gm d’acide malonique et 40ml de solution d’ammoniac éthanolique à 8% placés dans un ballon à fond rond de 100ml équipé d’un condenseur à reflux sur bain-marie jusqu’à obtention d’une solution claire (environ 8-10h). Régler l’ensemble pour une distillation descendante et éliminer par distillation l’excès d’alcool. Continuer à chauffer la partie huileuse résiduelle jusqu’à ce que le dégagement de gaz carbonique cesse. Dissoudre le résidu dans 20ml d’eau, refroidir et ajouter de l’acide chlorhydrique dilué jusqu’à ce qu’il soit acide. Recueillir l’acide insaturé précipité dans un entonnoir Buchner, laver à l’eau froide. Recristalliser à partir d’eau chaude et recueillir les cristaux d’acide cinnamique, m.p 132°C.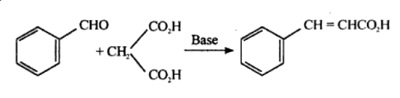
Synthèse de l’acide cinnamique à partir du benzaldéhyde
Analyse du contenu
Peser précisément 500 mg d’échantillon qui ont été préalablement séchés pendant 3 heures dans un séchoir rempli de gel de silice ; ajouter 0,1mol/L d’hydrogène.
Toxicité
GRAS (FEMA).
La DL50 orale aiguë chez le rat est de 2,5 g/kg, et la DL50 cutanée aiguë chez le lapin dépasse 5 g/kg. L’acide cinnamique appliqué pur sur une peau de lapin intacte ou abrasée pendant 24 h a été légèrement irritant;une solution à 4 % dans la vaseline n’a produit aucune sensibilisation chez l’homme.
Utilisation limitée
FEMA (mg/kg) : Boissons gazeuses 31 ; Boisson froide 40 ; Confiserie 30 ; Boulangerie 36 ; Gomme 10.
Prendre modéré comme limite (FDA§172.515, 2000).
Méthode de production
La synthèse commerciale de l’acide cinnamique donne presque toujours l’isomère trans.
La réaction de Perkin est la plus ancienne méthode connue de production commerciale de l’acide cinnamique. Dans cette réaction, le benzaldéhyde est condensé avec l’anhydride acétique en présence d’acétate de sodium comme catalyseur.
Le chlorure de benzal réagit avec l’acétate alcalin en milieu alcalin pour donner un rendement élevé d’acide cinnamique. L’acide cinnamique peut être obtenu par cette réaction en présence d’amines telles que la pyridine avec un rendement supérieur à 80 %.
Il peut également être préparé par : le mélange de la benzoylacétone, du carbonate de sodium et de l’eau de Javel, générant de l’acide cinnamique sodique, suivi d’un traitement au sulfate.
Description
L’acide cinnamique est un acide organique cristallin blanc, légèrement soluble dans l’eau.
Il est obtenu à partir de l’huile de cannelle, ou de baumes comme le storax. On le trouve également dans le beurre de karité et c’est la meilleure indication de son histoire environnementale et des conditions post-extraction. Il peut également être fabriqué synthétiquement.
L’acide cinnamique est utilisé dans les arômes, l’indigo synthétique et certains produits pharmaceutiques, bien que sa principale utilisation soit la fabrication des esters méthylique, éthylique et benzylique pour l’industrie du parfum. L’acide cinnamique a une odeur de miel ; il est, avec son ester éthylique plus volatil (cinnamate d’éthyle), un composant aromatique de l’huile essentielle de cannelle, dont le cinnamaldéhyde est le principal constituant. L’acide cinnamique fait également partie des voies de biosynthèse du shikimate et du phénylpropanoïde. Sa biosynthèse est réalisée par l’action de l’enzyme phénylalanine ammonia – lyase (PAL) sur la phénylalanine.
L’acide cinnamique est librement soluble dans le benzène, l’éther diéthylique, l’acétone, et il est insoluble dans l’hexane.
L’acide cinnamique est également une sorte d’auto-inhibiteur produit par les spores fongiques pour empêcher la germination.
Propriétés chimiques
L’acide cinnamique est presque inodore avec un goût de brûlé, puis devenant doux et rappelant l’abricot.
Occurrence
La forme trans- a été trouvée parmi les constituants des huiles essentielles de basilic, cannelle chinoise,Melaleuca bracteata, Alpinia galanga. Il est signalé trouvé dans le baume du Pérou, la storax asiatique et américaine et les feuilles de cacao. On le trouve également dans les fraises, la bière, le cognac, la carambole (Averrhoa carambola L) et le loquat. La forme cis- est présente dans l’huile d’Alpinia malacensis.
Usages
parfum & agent aromatisant, antidiabétique
Usages
l’acide cinnamique a des capacités de protection solaire. Certains fabricants l’utilisent pour remplacer le PABA en raison de sa moindre incidence de réactions allergiques et phototoxiques. L’acide cinnamique se trouve dans les feuilles de cannelle et les feuilles de cacao, et est une huile essentielle de certains champignons. Il peut provoquer des éruptions cutanées allergiques.
Utilisations
L’acide cinnamique est un agent aromatisant qui consiste en des écailles cristallines, de couleur blanche, avec une odeur ressemblant au miel et aux fleurs. il est légèrement soluble dans l’eau, soluble dans l’alcool, le chloroforme, l’acide acétique, l’acétone, le benzène et la plupart des huiles, et les sels alcalins solubles dans l’eau. il est obtenu par synthèse chimique. il est également appelé acide 3-phénylpro-pénoïque.
Définition
ChEBI : Acide monocarboxylique qui consiste en un acide acrylique portant un substituant phényle en position 3. On le trouve dans Cinnamomum cassia.
Préparation
Il existe deux isomères, trans- et cis- ; l’isomère trans présente un intérêt pour une utilisation en arômes ; outre l’extraction à partir de sources naturelles (storax), il peut être préparé comme suit : (1) à partir de benzaldéhyde, d’acétate de sodium anhydre et d’anhydride acétique en présence de pyridine (réaction de Perkin) ; (2) à partir de benzaldéhyde et d’acétate d’éthyle (condensation de Claisen) ; (3) à partir de benzaldéhyde et de chlorure d’acétylène ; (4) par oxydation de benzylidène acétone avec de l’hypochlorite de sodium.
Référence(s) de synthèse
Journal of the American Chemical Society, 75, p. 1068, 1953 DOI : 10.1021/ja01101a016
The Journal of Organic Chemistry, 59, p. 710, 1994 DOI : 10.1021/jo00083a006
Profil de sécurité
Poison par voie intraveineuse et intrapéritonéale. Modérément toxique par ingestion. Irritant pour la peau. Liquide inflammable. Lorsqu’il est chauffé jusqu’à décomposition, il émet une fumée et des émanations âcres.
Synthèse chimique
Rainer Ludwig Claisen (1851-1930), chimiste allemand, décrit pour la première fois en 1890 la synthèse des cinnamates en faisant réagir des aldéhydes aromatiques avec des esters. Cette réaction est connue sous le nom de condensation de Claisen.
Méthodes de purification
Cristalliser l’acide à partir de *benzène, CCl4, eau chaude, eau/EtOH (3:1), ou EtOH aqueux à 20%. Le sécher à 60o sous vide. Il est volatile à la vapeur.