Le mécanisme par lequel la réaction de Wohl-Ziegler se déroule a été proposé par Paul Goldfinger en 1953, et son mécanisme de réaction est l’une des deux voies proposées par lesquelles se produit la bromation aliphatique, allylique et benzylique avec le N-bromosuccinimide (NBS). Il a été démontré que le mécanisme de Goldfinger est le mécanisme approprié par opposition au mécanisme précédemment accepté proposé par George Bloomfield, qui, bien que cohérent pendant les études de sélectivité, s’est avéré être trop simpliste.
La génération de radicaux NBS représentée dans le mécanisme de Bloomfield s’est avérée beaucoup plus difficile que ce qui avait été imaginé lorsqu’il a été proposé, ce qui explique pourquoi il a échoué en tant que modèle approprié au fil des années ; cependant, des preuves suggèrent que le mécanisme de Bloomfield est toujours acceptable pour l’oxydation des alcools en utilisant le NBS. Dans le mécanisme de Goldfinger, le but de la NBS est simplement de maintenir une très faible concentration de brome moléculaire, tandis que dans le mécanisme de Bloomfield, son but est de générer le radical initial utilisé dans la réaction, ce qui, là encore, peut être un processus assez difficile. En effet, il faut tenir compte du comportement du radical NBS ; la seule façon dont il peut fonctionner comme le propose le mécanisme de Bloomfield est que l’énergie de dissociation de la liaison N-Br dans le NBS soit inférieure à celle du Br2, et de nombreuses preuves suggèrent un comportement contraire. Le mécanisme proposé par Goldfinger ne nécessite aucune considération particulière, car toutes les espèces radicalaires se comportent normalement, et c’est en partie pour cela que son mécanisme est considéré comme correct.

Pour approfondir le mécanisme réactionnel accepté, il faut comprendre qu’il existe des voies radicalaires concurrentes dans toute réaction radicalaire ; il en est de même dans ce cas, puisque les voies d’addition et de substitution sont concurrentes. Pour obtenir le produit bromé souhaité, il faut que la voie de substitution soit dominante, et les conditions de réaction peuvent effectivement être manipulées pour favoriser cette voie par rapport à la voie d’addition, moins souhaitable. Affiché ci-dessous sont les deux voies dans leur intégralité ; il y a des réactions secondaires inclus dans cette figure pour des raisons d’exhaustivité, comme les étapes 6 et 8 ; ces voies sont générales pour presque toutes les réactions radicalaires, donc NBS n’est pas représenté ici, mais son rôle sera discuté ci-dessous.
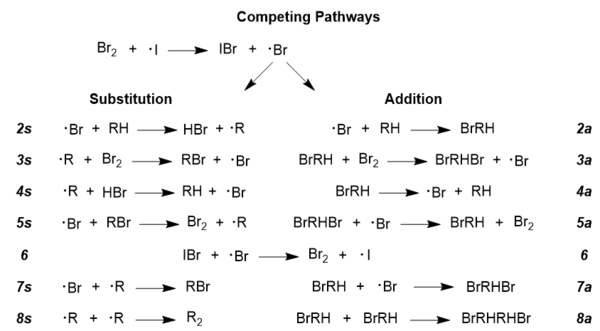
Le rôle du NBS dans le mécanisme de Goldfinger est de favoriser la régénération du brome moléculaire, mais l’un des avantages supplémentaires de l’utilisation du NBS est qu’il maintient une faible concentration de brome moléculaire, ce qui est essentiel pour favoriser la substitution par rapport à l’addition. Des lois de taux ont été développées qui décrivent le comportement compétitif de cette réaction, et elles montrent une forte dépendance à la concentration de brome moléculaire ; données ci-dessous sont les deux équations : une pour les concentrations élevées de brome et une pour les concentrations faibles de brome.
- Hautes concentrations de brome : r(a/s) = k2a/k2s(1 + k4a/k3a) où r(a/s) est le rapport entre l’addition et la substitution, et les valeurs de k correspondent aux constantes décrivant les étapes spécifiques de la réaction illustrées ci-dessus sous Voies concurrentes.
- Faibles concentrations de brome : r(a/s) = k2ak3a/k2sk4a où les termes ont la même définition que dans l’équation précédente. On peut voir que dans l’équation pour les faibles concentrations de brome, le rapport entre l’addition et la substitution est directement proportionnel à la concentration de brome moléculaire, donc la diminution de la concentration de brome inhiberait la voie d’addition et favoriserait un plus grand degré de formation de produits bromés.