
画像です。 “Circles” by Susanne Nilsson. License: CC BY-SA 2.0
ケトン体の種類と働き
私たちの体は3種類のケトン体で構成されています
- アセト酢酸は肝臓の代謝産物です。 アセトンやβ-ヒドロキシ酪酸に変換されます。
- アセトンは、アセトアセテートの自発的な脱炭酸やアセトアセテート脱炭酸酵素の作用によって生成されます。 呼気や尿に含まれて排出されます。 アセトンは、代謝を調節する役割はありません。
- β-ヒドロキシ酪酸は厳密にはケトン体ではなく、D-β-ヒドロキシ酪酸デヒドロゲナーゼの作用によりアセトアセテートから得られます。 最も豊富なケトン体である。
アセト酢酸とβ-ヒドロキシ酪酸は、肝細胞のミトコンドリアマトリックスで合成されます。 アセト酢酸とβ-ヒドロキシ酪酸は、肝細胞のミトコンドリアマトリックスで合成され、膜を通過しやすいため、脳や心筋、骨格筋などでは、グルコース濃度が低下したときにこれらの物質が再変換されることに依存しています。 脳は、血液脳関門が脂肪酸を透過しないため、エネルギー生成に脂肪酸を使用できず、絶食時にはケトン体を唯一のエネルギー源としている。 ケトン体を利用することで、脳が必要とするブドウ糖の量を平均150g/日から50g/日に減らすことができます。
ケトン体合成の活性化
生化学的には、長期間の絶食や飢餓状態のように、アセチル-CoA(ケトン体合成の出発物質)が増加すると、ケトン体の合成が促進されます。
糖尿病でもアセチル-CoAが蓄積されます。インスリンの分泌量が低下したり、インスリン抵抗性が高くなると、脂肪酸の分解が進み、アセチル-CoAが多く生成されます。 アセチル-CoAは、クエン酸サイクルの第一反応に必要なオキサロ酢酸が十分にある場合にのみ、クエン酸サイクルに入ることができます。しかし、糖尿病では、血液中のグルコースの細胞への吸収が阻害されるため、解糖の活性が低下し、ピルビン酸とオキサロ酢酸の産生が減少します。
つまり、糖尿病患者はアセチルCoAの量が増え、同時にオキサロアセテートが不足するため、アセチルCoA経路やHMG-CoA経路を介したケトン体の合成が活発になるのです。 また、ロイシンなどのケトジェニックなアミノ酸を脱アミノ化することで、クレブスサイクルに必要なオキサロアセテートの量を増やそうとする試みもあります。 ケトン体の合成は主に肝細胞のミトコンドリアで行われます。
アセチル-CoAの供給
アセチル-CoAは様々な代謝経路の産物です:
- 脂肪酸の分解では、β酸化のサイクルごとに1個のアセチル-CoAが生成されます。
- 解糖系の主要産物であるピルビン酸は、ピルビン酸デヒドロゲナーゼでアセチル-CoAに分解されるか、ピルビン酸カルボキシラーゼでオキサロ酢酸に分解され、最終的にはクエン酸サイクルに入ります。
- アセチル-CoAは、ケトジェニックアミノ酸と呼ばれる特定のアミノ酸を分解する際にも生成されます。
ケト新生
第1ステップ
まず、チオラーゼという酵素の作用により、2個のアセチル-CoAが縮合してアセトアセチル-CoAが生成されます。
ステップ2
次のステップでは、β-ヒドロキシ-β-メチルグルタリル-CoA合成酵素(HMG-CoA合成酵素)が触媒となり、水を使ってアセトアセチル-CoAのβ炭素にもう1分子のアセチル-CoAを加えます。
このステップでは、β-ヒドロキシ-β-メチルグルタリル-コエンザイムA(HMG-CoA)が生成されます。このコエンザイムAは、分岐した6つの炭素を持つ化合物で、細胞質でコレステロールを合成する際の中間体となります。
ステップ3
1つのアセチル-CoAがHMG-CoAリアーゼによって切断され、アセトアセテートが生成される。
ステップ4
アセトアセテートは、D-β-ヒドロキシブチレートデヒドロゲナーゼによってNADH+H+依存的にD-β-ヒドロキシブチレートに還元されるか、または自発的に脱炭酸反応を起こしてアセトンになります。
β-ヒドロキシ酪酸は、絶食や飢餓状態の時に最も血中濃度が高くなるケトン体です。
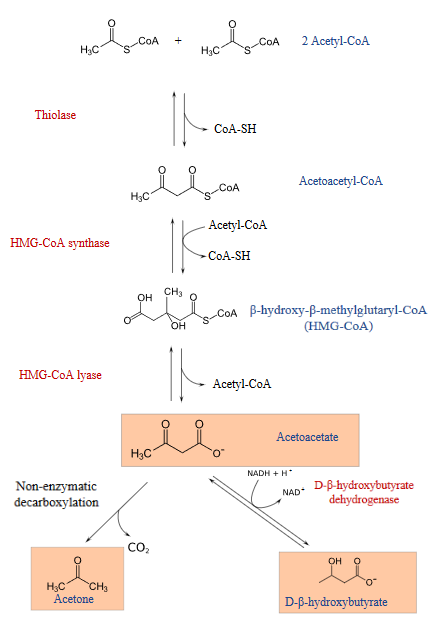
Image: “ケト生成経路 “とは 3つのケトン体(アセトアセテート、アセトン、β-ヒドロキシブチレート)はオレンジ色の箱の中に記されている」 by Sav vas. License: CC0 1.0
ケトン体の取り込み
生成されたケトン体は、血流に乗って目的の組織に向かいます。 脳はモノカルボン酸トランスポーター(MCT)の助けを借りてケトン体を利用します。MCTはアストロサイトや神経細胞の内皮細胞の細胞膜などに存在し、ピルビン酸に還元される乳酸の輸送も担います。
ケトン体の利用
ケトン体は、肝臓以外の全身(特に脳)で利用することができます。
ステップ1と2
利用の第1ステップでは(既に発生している場合を除く)、β-ヒドロキシ酪酸が酸化されて、血中で2番目に多いケトン体であるアセト酢酸になります。 これはNAD+依存性の反応で、β-ヒドロキシ酪酸デヒドロゲナーゼによって触媒されます。
ステップ2では、アセトアセテートは次の2つのメカニズムのうちの1つによってアセトアセチル-COAに活性化されます:
- 3-ケトアシル-CoAトランスフェラーゼは、クエン酸サイクルの副産物であるコハク酸のCoA基をアセトアセテートのカルボキシル基に転移させ、アセトアセチル-CoAとコハク酸を生成します。
- アセトアセチル-CoA合成酵素の触媒作用により、CoAはATP依存的にアセトアセテートのカルボキシル基と反応し、水、ATP、アセトアセチル-CoAを生成します。
第3ステップ
最終ステップでは、アセトアセチル-CoAは1のCoAを用いてチオラーゼにより切断され、2のアセチル-CoAが生成されます。
アセチル-CoAは、クエン酸サイクルでのエネルギー生産や、呼吸鎖を動かすために必要な還元性等価物の合成に利用できるようになります。
ケトアシドーシス
血液のpH値が< 7.35の状態をアシドーシスと呼びます。 ケトアシドーシスは、ケトン体の血中濃度が高いために起こるアシドーシスです。
3種類のケトン体はいずれも酸性であり、すなわち血中pHの低下を引き起こし、アシドーシスを生じさせます。
3種類のケトン体はいずれも酸性であり、血液のpHを低下させてアシドーシスを引き起こします。
レクチュリオで医学部や学会の勉強をしましょう。
- USMLE Step 1
- USMLE Step 2
- COMLEX Level 1
- COMLEX Level 2
- ENARM
- NEET