化学式Mg(NO3)2またはMgN2O6で表される硝酸マグネシウム(IUPAC名はmagnesium dinitrate)は、水やアルコールに溶ける吸湿性のある白色の結晶性粉末です。 これはマグネシウムの塩であり、イオン性の化学結合を含んでいます。

硝酸マグネシウム
硝酸マグネシウムの識別 |
|
| CAS番号 | 10377-?60-3 |
| PubChem CID | 25212 |
| ChemSpider ID | 23415 |
| EC番号 | 233-826-7 |
組成と合成
硝酸マグネシウムは、硫酸マグネシウムと硝酸カルシウムを組み合わせて調製することができます。
MgSO4 + Ca(NO3)2 = Mg(NO3)2 + CaSO4
硝酸マグネシウムの式
硝酸マグネシウムの性質と特徴 硝酸マグネシウム
General プロパティ |
||
| モル質量/分子量 | 148.313g/mol | |
物理的性質 |
||
| 色・外観 | 白色の結晶 | |
| 融点・凝固点 | 89℃, 192.2°F | |
| 沸点 | 330°C, 626°F | |
| 強度 | 1.46g cm-。3 | |
| 室温での物質の状態(通常の相) | 固体 | |
化学的な プロパティ |
||
| 水への溶解度 | 42 g/100ml (at 20oC) | |
| pH | 5-。7 (酸性) | |
原子の特性 |
||
| 結晶 構造 | Cubic | |
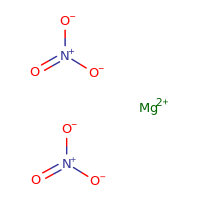
硝酸マグネシウムの構造
Mg(NO3)2の代表的な反応
硝酸マグネシウムと炭酸ナトリウムを化学反応させると、炭酸マグネシウムと硝酸ナトリウムが生成されます。
Mg(NO3)2 + Na2CO3 = MgCO3 + 2NaNO3
硝酸マグネシウムは水中で分解して水酸化マグネシウム、アンモニア、酸素を生成します。
Mg(NO3)2 + 4H2O = Mg(OH)2 + 2NH3 + 4O2
Mg(NO3)2を加熱すると、酸化マグネシウム、二酸化窒素、酸素に分解します
2Mg(NO3)2 = 2MgO + 4NO2 + O2
水酸化ナトリウムと反応して、水酸化マグネシウムと硝酸ナトリウムを生成します。
Mg(NO3)2 + 2NaOH = Mg(OH)2 + 2NaNO3
硝酸マグネシウムの用途
- 硝酸イオンの安全な供給源として
- 窒素肥料の生産に
- 火工品や濃硝酸の製造に
- 役立つ。
- 硝酸アンモニウム製造のためのプリリングやコーティングに役立ち、化粧品やシャンプーの成分となる。
危険有害性
強い酸化剤であるため、火災の原因となる。 また、有機物と接触すると爆発の危険性がある。 目や皮膚に触れたり、吸い込んだりすると、刺激、咳、息切れなどの症状が出るので避けなければならない。
- 硝酸マグネシウム – Pubchem.ncbi.nlm.nih.gov
- 硝酸マグネシウム – Chemspider.com
- Magnesium Nitrate – Americanelements.com
- Magnesium Nitrate – Sciencemadness.org
- Magnesium Nitrate Hexahydrate – Sigmaaldrich.com
- Magnesium Nitrate – Chemicalbook.com
- 質問があります。 硝酸マグネシウムと炭酸ナトリウム Mg(NO_3)_2 + Na_2 – Chegg.com
- 硝酸マグネシウムと水の平衡式はどのようにして決まりますか? – Quora.com
- 硝酸マグネシウムの熱分解について – Chemiday.com
- 質問です。 水酸化ナトリウムは硝酸マグネシウムと反応して水酸化マグネシウムになる – Chegg.com