はじめに
慢性閉塞性肺疾患(COPD)は、全身に影響を及ぼしながらゆっくりと進行する重篤な肺疾患で、主に40歳以上の方が罹患しています1。 しかし、COPDは予防も治療も可能であり、多くの患者がCOPDの増悪を経験し、その中には緊急治療室(ER)の受診や入院を必要とするものもあります。 ポルトガルでは、2009年から2016年の間にCOPDによる入院は8%減少しましたが、2016年の入院患者数は8049人でした。
COPDの増悪を適切に管理することは、重要な臨床的課題です。3 COPD増悪の70~80%では呼吸器感染症が誘因となっていますが4、COPDの重度増悪の約3分の1では原因が特定できず1、治療戦略の適切な指針となることができません。 増悪とその重症度を評価するための診断ツールはいくつかありますが、これは、患者が自宅やプライマリーケアで管理できるのか、あるいはERに紹介して最終的に入院させるべきなのかといった判断に役立ちます1,5-7。増悪の重症度はその治療に影響を与えますが、1,7,8、また、将来の増悪のリスクを予測するために予後スコアを使用する必要があります。 増悪の生物学的および臨床的特徴に基づいて、3つの予後スコアが提案されています:BAP-65スコア9、DeCOPDスコア9、およびRocheらによって提案されたスコア10,11
増悪が適切に管理された後、適切な退院計画を準備する必要があります。 増悪の重症度にもよりますが、一般的にはGOLD基準による患者の再分類、1 薬物療法の最適化、1,4,8 併存疾患の管理、薬の正しい使い方に関する患者(または家庭の介護者)の教育、1,8 まだ呼吸器科に通っていない場合は呼吸器科への紹介、禁煙と肺のリハビリテーションプログラムなどが含まれます。
増悪の定義、原因、病因Diffinition
現在、COPD増悪の正確で一貫した定義はありません。 2016年のGOLDアップデートにおける増悪の定義12「通常の日内変動を超える患者の呼吸器症状の悪化を特徴とし、投薬の変更をもたらす急性の出来事」は、GOLD2017年の文書13では「追加治療をもたらす呼吸器症状の急性の悪化」と簡略化されています。
原因と病因
症状の悪化をもたらすいくつかの要因が特定されており、COPD増悪の70~80%では、前駆要因として呼吸器感染症4、ウイルス性4,9,14,15または細菌性4,9,15が挙げられますが、COPDの重度増悪の約3分の1では原因が特定できません1。
治療戦略の指針となるため、増悪の根本的な原因を特定することは重要です。
Classification
増悪の定義がないのと同様に、増悪の重症度を評価する合意された分類システムはありませんが、いくつか提案されています16。
軽度の増悪では、症状の悪化が見られますが、常用薬の量を増やすなどして、自宅で管理することができます。 中等度の増悪では、気管支拡張剤の増量に反応しないため、全身性コルチコステロイドおよび/または抗生物質による治療が必要となります。1,6,17,18 重度の増悪では、入院またはERでの評価が必要となり1,6,17,18、身体活動に深刻な影響を及ぼします。 非常に重度の増悪では、集中治療室(ICU)1 への入院が必要となり、身体活動への影響も非常に大きくなります。 感染性増悪は、呼吸困難の悪化に伴う痰の量と膿の増加を特徴とし、抗生物質で治療する必要があります1,8。 息切れ、咳や痰などの症状、7 酸素飽和度、7 日常生活の新たな制限、6,7 呼吸補助筋の使用、1,5 逆説的な胸壁の動き、1,5 中心性チアノーゼの悪化または新たな発症、1,7 末梢性浮腫の発症、1,7 血行動態の不安定さ、1 精神状態の悪化1,6,7 および併存疾患1 など、重症度を示す臨床症状をすべて評価する必要があります。 患者が病院に紹介された場合は、動脈血ガスを測定し5,6,8,15,19-21、併存疾患や他の肺疾患を除外するために胸部X線撮影を行う必要があります1,6,8,15,19。 これらのケースでは、心電図、1,6,19,20全血球数、1,6,8,20-22、電解質濃度、1,8,20,21尿素、8血糖値1,20、メタボリックパネルなどの基本的な生化学検査を行うことが推奨されています6。 8 喀痰の培養は日常診療では推奨されておらず、喀痰が膿性の場合のみで、8 GOLD 2018の文書では、感染性増悪が経験的抗生物質治療に反応しない場合にのみ、喀痰の培養と抗生物質感受性試験を推奨しています1。 一部の著者は、好酸球性の増悪は全身性ステロイドに反応する可能性が示唆されていることから、COPD増悪治療の指針となる望ましい処置として好酸球血算に言及しています1,15。増悪中のスパイロメトリーは推奨されていません1
増悪が重篤で患者が入院している場合、特に従来の治療に反応しない場合は、脳性ナトリウム利尿ペプチドや心筋酵素測定値を考慮する必要があります6。 プロカルシトニンは、細菌感染症のより特異的なマーカーとして示唆されており、抗生物質の処方を決定する上で有用であると考えられます1。 Charlson comorbidity index,5,20,21,23 modified Medical Research Council (mMRC) dyspnea scale,5,20,21,23 physical activity5 and general health5 を評価すべきである。 COPD Assessment Test(CAT)スコア23は、ポルトガルの人口に対して検証されていないため、著者らはポルトガルで日常的に使用することを勧めていない。 患者がICUに入院した場合、重度の増悪時に推奨される検査以外に、グラスゴー・コーマ・スケール5を使用し、呼吸器感染症を調べ25、血液培養を行うべきである24。
Pharmacologic strategiesLABA+LAMA
短時間作用型吸入β2アゴニスト(SABA)と短時間作用型ムスカリンアンタゴニスト(SAMA)は、COPD増悪時の症状と気流の閉塞に対する治療の主役であり続けています1,4,6。 GOLD2018年版文書の発表時点では、増悪時における長時間作用型β2作動薬(LABA)または長時間作用型ムスカリン拮抗薬(LAMA)の有用性を評価した臨床研究はありませんでしたが、増悪時にこの薬を継続するか、退院前のできるだけ早い時期に開始することが推奨されています1。 LABAとLAMAの併用療法は、COPDの安定期にある患者に処方された場合、増悪を抑制する効果があることが証明されています26。特に、SPARK27およびFLAME28試験で実証されたように、インダカテロールとグリコピロニウムの併用療法は、増悪を抑制する効果があります。 さらに、治療効果のバイオマーカーとして血中好酸球増加症を評価した初めての前向き試験であるFLAME試験28では、分析したすべてのカットオフ値において、インダカテロール/グリコピロニウムがサルメテロール/フルチカゾンと比較して肺機能を有意に改善することが示されました29。 実際、最新版のGOLD文書1によると、COPDの安定期にあり、過去1年間に2回以上の中等度の増悪、または1回の入院歴がある症状のある患者は、LABA/LAMAに加えてICSを使用することが有益であるとされています。 しかし、WISDOMのpost hoc analysisで示唆されているように、血中好酸球が増悪予防の観点からICSの有効性を予測するバイオマーカーとして使用できるかどうかは、まだ確立されていません1。
抗生物質、コルチコステロイド、キサンチン
増悪を治療する際には、症状の重症度や感染症の有無に応じて、経口または静脈内のコルチコステロイドおよび/または抗生物質を追加することが推奨されます1,4,6-8,31。 GOLD 2018およびNHS 2014の文書では、呼吸困難、痰の量、痰の膿みの増加という3つの基本的な症状があるCOPD増悪患者7(エビデンスB)1、基本的な症状が2つあり、痰の膿みの増加が2つの症状のうちの1つである場合7(エビデンスC)1、または人工呼吸(侵襲的または非侵襲的)を必要とする患者(エビデンスB)に対して、抗生物質の投与を推奨しています。1
抗生物質は、短期死亡率、治療失敗、痰の膿みのリスクを減少させることが示されています。また、機械的換気(侵襲的または非侵襲的)を必要とする増悪を伴うCOPD患者を対象とした研究では、抗生物質による治療を行わないことは、死亡率の増加と二次的な院内肺炎の発生率の増加に関連することが示されました1。 コクラン・レビューでは、非常に重篤なCOPDの増悪に対する抗生物質の投与は、ICUに入院した患者のアウトカムに広く一貫した有益な効果を示すと結論づけていますが32、この結論は1つの研究から得られたデータに基づいています。 しかし、19のCOPDガイドラインを対象としたシステマティックレビューでは、抗生物質で患者を治療する基準は主に呼吸器症状の増加に基づいており、一方で全身性副腎皮質ステロイドは急性増悪のすべての患者に普遍的に推奨されることが多いと報告されています33。 また、現在のCOPDガイドラインは、プライマリーケアにおいて全身性副腎皮質ステロイドと抗生物質による治療が有効である可能性が高い急性増悪患者を特定する上でほとんど役に立たず、どちらかの治療の過剰使用や不適切な使用の一因となっている可能性があると結論づけています。
抗生物質治療の最適化に有用なバイオマーカーがいくつか提案されています。 GOLD 2018の文書1では、CRPを日常的に使用することは推奨していませんが、いくつかの研究で、プロカルシトニン誘導による抗生物質治療は、同じ臨床効果で抗生物質の曝露と副作用を減らすことが示唆されていると述べています。 一方、他の著者は、CRPの方がより価値のあるマーカーであるかもしれないと報告しており34、実際のプライマリーケアの研究では、CRP迅速検査を行うことで、一般開業医が処方する抗生物質の量が、行わない場合に比べて少なくなると結論づけています35。
すべての患者に対して、抗生物質の選択は、その地域の細菌の耐性パターン、1,8 患者の微生物学的ストーリーとそのリスク要因に基づいて行う必要があります。
通常、初期の経験的治療は、クラブラン酸を含むアミノペニシリン、マクロライド系、またはテトラサイクリン系を含みます。 しかし、マクロライド系抗菌薬の長期使用は、重要な副作用や耐性菌発生のリスクを伴う可能性があります36。また、頻繁に増悪する患者、重度の気流制限がある患者、機械的換気が必要な増悪がある患者1の場合は、グラム陰性菌(Pseudomonas speciesなど)や上記の抗生物質に感受性のない耐性菌が存在する可能性があるため、喀痰を培養に回す必要があります1。
最も効果的な治療期間はまだ定義されていませんが、32 抗生物質治療の推奨期間は通常5~7日(エビデンスD)1ですが、治療期間は使用する抗生物質によって異なります。
プライマリーケアにおける増悪の管理は、気管支拡張剤治療を最大限に行い、禁忌でなければ全身性コルチコステロイド(プレドニゾロン30mg)を7日間投与することです1,7,8。 プレドニゾロンの経口投与による治療は、静脈内投与と同等の効果があるとされています1。 GOLD 2018の文書では、プレドニゾン1日40mgを5日間投与することが推奨されています1が、NICE 2016では、30mgを7~14日間投与することが推奨されており、さらに、副腎皮質ステロイド治療を長期化しても利点がないことから、1コースを14日以上にしないことが推奨されています8。 COPD増悪時に全身性コルチコステロイドを使用することで、回復時間の短縮、肺機能の改善、酸素化の向上、早期再発や治療失敗のリスクの減少、入院期間の短縮などの効果が確認されています1
メタアナリシスでは、COPD増悪時の通常のケアと比較して、全身性コルチコステロイドを使用することで治療成功率が上昇することが確認されています。 コルチコステロイドは、治療成功率という点では、集団全体に有益であると思われます。37
血中好酸球のレベルが低い患者では、コルチコステロイドのCOPD急性増悪に対する効果が低い可能性を示唆する研究もあります15,38。
COPD増悪の管理におけるメチルキサンチンについては、肺機能や臨床エンドポイントにおける有益な効果の可能性は控えめで一貫性がなく、有害事象も大きいことから、現在のエビデンスではその使用を支持するものではありません1,4,6,31。 テオフィリンを使用する際には、血中濃度、副作用、潜在的な薬物相互作用をモニターする必要があります8,31。
先に述べたように、COPDの増悪は非常に異質であるため、その病因、病態、重症度、リスクを見極めることが特に重要となります。
薬理学的治療と治療場所に関しては、増悪が軽度で非感染性の場合、1,4,7,8,31 自宅で維持用気管支拡張剤の用量を増やして治療することができます。 もし増悪が感染性であれば4,8,31 抗生物質を投与すべきである。1,7
中等度の増悪は、社会経済的な理由で入院する場合を除き、入院を必要としないので、ERで治療し、患者は退院すべきである。 1,38,39 もし増悪が感染性のものであれば4,8,31 抗生物質を投与すべきである。1,7
入院を必要とする重度の増悪を起こした患者の場合、その患者は頻繁に増悪を起こす患者として再分類されるべきである。 通常、重度の増悪による入院では、患者が低酸素血症の場合は酸素を、52cmH2O以上の過呼吸および/または酸血症の場合は非侵襲的換気を含む吸入維持療法の変更が必要となります1,4,6,8経口または静脈内コルチコステロイド(5日間)1,38,39、感染性の場合は抗生物質、1,7治療への反応が不十分な場合はキサンチン系薬剤4,8,16,31、および肺血栓塞栓症の予防が必要となります。
退院-行動計画
軽度の増悪を起こした患者は、3ヵ月後にスパイロメトリーとGOLD度の再評価を行い、必要に応じて再分類を行う必要があります。
中等度の増悪からの退院時には、気管支拡張を最適化し、抗肺炎球菌ワクチンを処方し、禁煙と呼吸リハビリテーションの計画を準備する必要があります。
重度の増悪からの退院時には、LABA、LAMA、ICSによる最適な維持療法1,4,8を処方する必要があります。 呼吸不全を起こしたことのある患者は、退院前にオキシメトリや動脈血ガスの結果が満足できるものでなければならない。 患者(または介護者)には、吸入器や酸素を含む薬剤の正しい使用方法を十分に理解できるように適切な情報を提供し、必要に応じてフォローアップや在宅ケア(訪問看護師、酸素供給、他のサポートの紹介など)の手配を行うべきである。 患者さん、患者さんの介護者、医師は、患者さんが新しい治療計画をうまく管理できることを確信する必要があります。 患者の治療管理能力に疑問がある場合は、正式な日常生活動作評価が役立つ場合があります。8 GOLD 2018文書には、退院基準のリストが記載されています。1 増悪時に低酸素血症になった患者については、退院前およびその後3カ月間に動脈血ガスおよび/またはパルスオキシメトリーを評価する必要があります。 1,8 個別ケアの必要性について、退院後の電話連絡、家庭訪問、継続的なケアを患者に提供したカナダの研究では、30日および90日の再入院率の低下は見られなかったものの、90日の総死亡率の低下が見られました。 これらのデータは、この研究で行われた個別のケアが、急性増悪後のCOPDの罹患率と死亡率に影響を与えることを示唆しています40。 重度の増悪を起こしたすべての患者は、退院後4~6週間後に再評価を受け、1 抗肺炎球菌ワクチンの処方を受け、禁煙と呼吸器リハビリテーションの計画を作成する必要があります-図1。
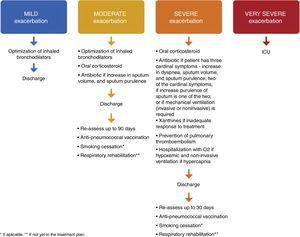
軽度、中等度、重度、非常に重度のCOPD増悪の提案された治療法、退院とフォローアップ
著者らは、ERや病院から退院した10~20日後に抗肺炎球菌ワクチンを処方することを提案しています。
フォローアップ診察時(中等度の増悪では3ヶ月、重度の増悪では4~6週間)には、スパイロメトリーと動脈血ガスを測定する必要があります。 症状、吸入療法の正しい使用、併存疾患の適切な管理を再評価する必要があります。 薬理学的治療は最適化されるべきである。 禁煙と呼吸器リハビリテーションの計画を評価すべきである。
結論
COPD増悪の根本的原因を特定し、その重症度を評価することは、治療の指針となる基本的なことです。 増悪を適切に管理した後は、その重症度に応じた適切な退院計画を準備する必要がある。 適切な退院計画は、症状の負担を減らし、早期回復に貢献し、患者さんの生活の質を高め、将来の増悪を予防または遅らせることができます。
Conflicts of interest
ARは、AstraZeneca、Boehringer Ingelheim、Novartis、Bial、Medinfar、Mundipharma、Menarini、Grifols、Mylan、Tecnifar、Teva、sslbehringから講演料を受け取っていることを表明しています。 CAは、AstraZeneca、Pfizer、Novartis、Mundipharmaから講演料を受け取ったことを表明しています。 SFは利益相反のないことを表明しています。 JFは、アストラゼネカ、ベーリンガーインゲルハイム、ダイアター、インムノテック、メナリーニ、ムンディファーマ、マイラン、テクニファール、TEVAから講演料を受け取り、バイアル、GSK、ノバルティスのアドバイザリーボードに参加していることを表明しています。 MDは、AstraZeneca社、Boehringher Ingelheim社、Bial社、GSK社、Menarini社、Novartis社から講演料を、Bial社、GSK社、Novartis社のアドバイザリーボードに参加していることを表明しています。 CRCは、Boehringer Ingelheim、Roche、Novartis、AstraZeneca、Pfizer vaccines、Teva、Menarini、Medinfar、Tecnifarからの講演料、Boehringer Ingelheim、Roche、Novartis、GSK、AstraZeneca、Pfizer vaccinesのアドバイザリーボードへの参加を表明しています
。