.jpg) アンモニアの製造は、世界の農業にとって非常に重要であり、アンモニアから窒素を含むすべての肥料が生産されます。
アンモニアの製造は、世界の農業にとって非常に重要であり、アンモニアから窒素を含むすべての肥料が生産されます。
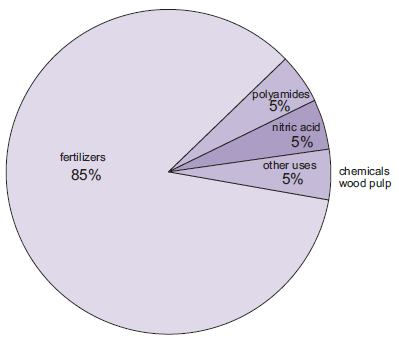
図1 アンモニアの用途。
他の用途に比べるとまだ少ないが、発電所から排出される窒素酸化物対策の濃縮液として使用されるアンモニアの量が増えている。
アンモニアの年間生産量
アンモニアは硫酸に次いでトン数の多い化学物質である。 天然ガスや石炭を安価に入手できる国での生産が増えている(中国とロシアが約40%を占める)。 最大規模のプラントでは日量約3000トンを生産しており、日量4000〜5000トンのプラントの建設が計画されているため、このようなプラントが100基あれば世界の総生産量を管理できることになります。 現在の生産量は
| 世界 | 1億4600万トン |
| 中国 | td 百万トン |
| ロシア | 1,200万トン |
| インド | 1,100万トン |
| U.S. | 900万トン |
| インドネシア | 500万トン |
| トリニダード・トバゴ | 500万トン |
| ウクライナ | 400万トン |
データは以下の通り。
U.U.S. Geological Survey, Mineral Commodity Summaries, 2016.
アンモニアの製造トン数の増加は、世界の人口増加と、その生活水準の向上に合わせたものです。 アンモニアの需要は、20181年には2億トン近くまで増加すると予想されています。
1.
アンモニアの製造
窒素と水素からのアンモニアの製造は、主に2つの段階で行われます:
a) 水素の製造
b) アンモニアの合成(ハーバープロセス)
水素の製造には、いくつかの異なるプロセスがあります。 図2は、その順序とアンモニアプラント内の位置(ステップ1~5)を示している。 また、水素からアンモニアを作るための変換器も示している(ステップ6)。 それぞれの工程で何が行われているかは、図の下で説明します。
|
図2 西オーストラリアにあるアンモニアプラントの様子。 1 脱硫装置 |
.jpg) |
(a)水素の製造
水素は様々な原料から製造されますが、主に天然ガス、石炭、ナフサなどから得られます。 これらの原料から水素を得る方法については、別途説明します。
天然ガス(メタン)からの水素
これには2つの段階があります。
i) 合成ガス(一酸化炭素と水素の混合物(水蒸気改質))の製造
ii) 一酸化炭素を除去し、水素と窒素の混合物(シフト反応)の製造
(i) 合成ガスの製造
いずれにしても、メタンには有機硫黄化合物や硫化水素が含まれているので、これらを除去する必要があります。 除去しないと、合成ガス製造に必要な触媒を害してしまうからです。 脱硫装置では、有機硫黄化合物をまず硫化水素に変えてから、酸化亜鉛と反応させることが多い。 このようにして得られた原料を水素と混合し、コバルトとモリブデンの混合酸化物を不活性な担体(特殊処理されたアルミナ)に担持させた触媒の上を約700Kで通過させます。
.jpg)
その後、ガスを酸化亜鉛の上に約700Kで通過させ、硫化水素を除去します。
.jpg)
一次水蒸気改質では、メタンと水蒸気を一酸化炭素と水素の混合ガスである合成ガスに変換します。
.jpg)
高温・低圧は生成物の形成に有利です(ル・シャトリエの原理)。 実際には、縦型のニッケル合金管の中に入れられた酸化カルシウム/酸化アルミニウム担体の表面に細かく分割されたニッケルの触媒の上に反応物を通過させます。 最大350本のチューブを並列に並べ、1000K以上の炉で約30気圧の圧力下で加熱します。
第二次水蒸気改質では、空気中の酸素と存在する水素の一部を反応させ、得られた混合物をニッケル触媒の上に流します。 燃焼時に発生する蒸気と熱により、残留するメタンの大部分が分解されます。
small.jpg)
この純発熱段階で発生するガスは約1200Kであり、熱交換器で冷却されます。
最近の設計では、二次改質器からの廃熱を直接一次改質器の熱源として利用するものもあります。
この段階では、ガスは水素、窒素、一酸化炭素、二酸化炭素を含み、約0.25%のメタンを含んでいます。
(ii) シフト反応
このプロセスでは、一酸化炭素を二酸化炭素に変え、さらに水素を生成します。
これは2段階で行われます。
これは2段階で行われます。1つ目の高温シフト反応では、ガスは蒸気と混合され、固定床反応器の中で約700Kの鉄/クロム(III)酸化物触媒に渡されます。
.jpg)
第2段階の低温シフト反応では、混合ガスを約500Kで銅・亜鉛触媒に通し、一酸化炭素濃度をさらに0.2%まで下げます。
この反応を2段階で行うのにはいくつかの理由があります。 この反応は発熱します。 しかし、高温では平衡制御のため、一酸化炭素の出口濃度はまだかなり高くなります。 低温段階で使用される銅触媒は高温に非常に敏感であり、高温段階では効果的に作動しない。 そのため、反応の大部分を高温で行い、熱のほとんどを回収する。
混合ガスには約18%の二酸化炭素が含まれていますが、これはいくつかの方法のうちの1つを用いて、塩基の溶液でガスをスクラブすることで除去します。
二酸化炭素を除去する方法としては、有機塩基(二酸化炭素吸収剤)、エタノールアミン(多くは2,2′-(メチルイミノ)ビスエタノール(N-メチルジエタノールアミン))の溶液が好まれます。 その多くは液化され、炭酸飲料、原子力発電所の冷却剤、温室での植物の成長促進などの目的で販売されています。
最後の炭素酸化物の痕跡は、ガスを600Kでニッケル触媒に通すことで除去されます。
このプロセスはメタネーションとして知られています。 典型的な組成のガスが得られます。
ナフサからの水素
ナフサを原料とする場合は、さらに改質工程が必要となります。 ナフサを加熱して蒸気にし、蒸気と混合してチューブに通し、750Kで加熱し、アルミニウムとマグネシウムの混合酸化物にニッケルを担持させた触媒を充填します。
石炭からの水素
石炭を使う場合は、まず細かく砕き、酸素と水蒸気の雰囲気の中で加熱する。
.jpg)
発生したガスは、約55%の一酸化炭素、30%の水素、10%の二酸化炭素、そして少量のメタンと他の炭化水素を含んでいます。
石炭を使用する際の主な問題点としては、石炭を燃やす際に発生する大量の二酸化硫黄や三酸化硫黄、ヒ素や臭素などのその他の不純物が大量に含まれていることが挙げられますが、これらはいずれも大気に非常に有害であり、プロセス中の触媒にとってはいずれも深刻な毒物です。
バイオマスからの水素
合成ガスはバイオマスから作ることができます。
(b) アンモニアの製造(ハーバープロセス)
.jpg)
このプロセスの中心は、固定床反応器での水素と窒素の反応です。
.jpg)
図3従来の合成反応器(コンバーター)を示す図
平衡混合物中のアンモニアの割合は、圧力の増加と温度の低下によって増加します(Le Chatelierの原理)。 量的なデータを表1に示す。 適度な収率と好ましい速度を得るためには、高い圧力、適度な温度、触媒を使用します。
| 圧力/atm | さまざまな温度での平衡状態におけるアンモニアの存在割合 | ||||||
|---|---|---|---|---|---|---|---|
| 373K | 473K | 573K | 673K | 773K | 973K | ||
| 10 | -。 | 50.7 | 14.7 | 3.9 | 1.2 | 0.2 | |
| 25 | 91.7 | 63.6 | 27.4 | 8.7 | 2.9 | – | |
| 50 | 94.5 | 74.0 | 39.5 | 15.3 | 5.6 | 1.1 | |
| 100 | 96.7 | 81.7 | 52.5 | 25.2 | 10.6 | 10.6 | 2.2 |
| 200 | 98.4 | 89.0 | 66.7 | 38.8 | 18.3 | – | |
| 400 | 99.4 | 94.6 | 79.7 | 55.4 | 31.9 | – | |
| 1000 | – | 98.3 | 92.6 | 79.8 | 57.5 | 12.9 | |
表1 温度と圧力の範囲で窒素と水素を反応させたときの平衡混合物に含まれるアンモニアの体積比
反応器の構造により、幅広い条件が使用されています。
反応器の構造により、さまざまな条件が用いられますが、温度は600~700K、圧力は100~200気圧が用いられます。
反応が発熱性であるため、反応器の温度を下げるために冷却剤(窒素と水素)を加える(図3)。
アンモニアは通常、現場で貯蔵され(ステップ7)、ポンプで工場の別の場所に送られ、そこで肥料(尿素またはアンモニウム塩)に変換される。
.jpg) |
図4 西オーストラリア州のプラントでは、アンモニアをパイプラインで近くの港に運び(図2、ステップ8)、船で輸送しています。 こちらは約4万トンの液化アンモニアを積んでいます。 By kind permission of Yara International ASA. |
ハーバーが使用した当初の触媒はFe3O4で、反応物である水素によって還元されて鉄になりました。
最近の研究では、より低い圧力と温度でプロセスを起こせるよう、さらに効果的な触媒を見つけることに焦点が当てられています。
.jpg)
図5 アンモニアの製造。
あとがき
ハーバープロセスは、私たちの生活にとって非常に重要なものですが、90年近くの間に3つのノーベル化学賞をドイツの科学者が受賞しているという、驚くべき記録があります。
2007年には、ゲルハルト・エートル氏が、固体上での気体反応の触媒作用に関する研究で受賞しました。
2007年にゲルハルト・エートルが受賞したのは、固体上での気体反応の触媒作用に関する研究でした。彼が研究した幅広い反応の中で、鉄の表面に窒素分子と水素分子が吸着し、これらの吸着分子が原子に解離するという証拠を得ました。 そして、これらの原子が段階的に結合して、アンモニア分子を形成する。
まとめ
メタンからアンモニアを製造するプロセスを図5にまとめてみました。 石炭やナフサを原料とする場合は、追加の工程が必要となる。 ナフサは一次改質器に入る前にメタンと炭素酸化物に変換され、その後、シフト反応に入る。 また、石炭は水素と炭素酸化物に変換され、この混合物がシフト反応を起こす。