Wprowadzenie
Choroby autoimmunologiczne stanowią szeroki wachlarz problemów klinicznych dotyczących wielu narządów i układów i dotykają co najmniej 5% populacji.1 Duża różnorodność przeciwciał została powiązana z różnymi objawami klinicznymi i klinicyści opierali się na nich przy ustalaniu rozpoznania klinicznego, implikacji prognostycznych, a w niektórych przypadkach także decyzji terapeutycznych.2,3 Aktualna wiedza na temat patogenezy chorób autoimmunologicznych jest zgodna, że do ich powstania konieczna jest złożona interakcja genów i cech środowiskowych.4
Połączenie liniowego testu immunoblot ENA (INNOLIA-ANA) i techniki immunofluorescencji pośredniej do wykrywania przeciwciał przeciwjądrowych w komórkach HEp-2 jako substracie jest dobrą metodą przesiewową u pacjentów z klinicznym podejrzeniem choroby autoimmunologicznej, głównie tocznia rumieniowatego układowego (SLE) i zespołu Sjögrena (SS). Chociaż mogą wystąpić wyniki fałszywie dodatnie, miana >1:80 sugerują możliwość zaburzeń autoimmunologicznych i powinny skłonić do zlecenia bardziej szczegółowych ocen w celu określenia specyficznych reaktywności przeciwciał przeciwjądrowych (ANA), takich jak przeciw dwuniciowemu DNA i ekstrahowalnym antygenom jądrowym (ENA).5
Ro/SSA i La/SSB są heterogennymi kompleksami antygenowymi utworzonymi przez trzy różne białka (Ro-52, Ro-60 i La) i cztery cząsteczki YRNA. Białko Ro60 działa jako punkt kontroli jakości dla źle złożonego RNA z chaperonami molekularnymi dla wadliwych RNA. Błędnie złożone RNA są rozpoznawane, a następnie znakowane przez Ro60 w celu degradacji. Ro52 oddziałuje z różnymi cząsteczkami, między innymi z kalretikuliną i białkiem wiążącym łańcuchy ciężkie immunoglobulin. Uważa się, że Ro52 może modyfikować rolę lub stabilność swoich substratów poprzez ubikwitynację, a ta modyfikacja może skutkować zdarzeniami biologicznymi, w których pośredniczy Ro52.6
Przeciwciała anty-Ro/SSA i anty-La/SSB zostały opisane w różnych chorobach autoimmunologicznych. W pierwotnym zespole Sjögrena (pSS) krążące przeciwciała wykrywa się u około 60-70% pacjentów, a wyższe ich stężenie wiąże się z wczesnym początkiem choroby i objawami ogólnoustrojowymi.7,8 Grupa badawcza GEMESS, obejmująca 12 ośrodków referencyjnych w Hiszpanii, potwierdziła te cechy kliniczne i laboratoryjne w kohorcie pacjentów z pSS i zaobserwowała obniżone stężenie C4 u pacjentów z wczesnym początkiem choroby.9
Anty-Ro/SSA wykrywa się u 30% pacjentów z rozpoznaniem SLE, szczególnie (90%) w podtypach o późnym początku, podostrym skórnym toczniu rumieniowatym, toczniu polekowym i wrodzonych niedoborach C2, C4 i C1q, a także u pacjentów z zespołem nakładania SS/SLE i niezróżnicowaną chorobą tkanki łącznej.10 Z kolei anty-La/SSB częściej wiąże się z SS,11 i silnie koreluje u osób z dodatnim anty-La/SSB i ujemnym anty-Ro/SSA z dysfunkcją narządową (nerki, płuca, wątroba).12
Od lat 80. opisywano rozwój wrodzonej blokady serca w chorobach autoimmunologicznych, takich jak SS i SLE. Jednak zajęcie serca jest bardziej związane z krążącymi przeciwciałami pochodzącymi od matki niż z rozpoznaniem choroby autoimmunologicznej. Chociaż profil immunologiczny jest zmienny w różnych badaniach, przeciwciała anty-Ro52 występują częściej u matek dzieci z wrodzoną blokadą serca, toczniem noworodkowym i noworodkami z wydłużonym QT bez wrodzonej blokady serca.10,13,14
Powszechność i związki kliniczne przeciwciał anty-Ro/SSA i anty-La/SSB mogą się różnić w różnych grupach etnicznych. Oprócz badań przeprowadzonych w populacji hiszpańskiej nad ekspresją immunologiczną SS, w ostatnich latach opracowano inne badania nad profilem immunologicznym pacjentów z przeciwciałami anty-Ro52, anty-Ro60 i anty-La. Większość z nich dotyczyła specyficznej diagnostyki zaburzeń tkanki łącznej. W kohorcie pacjentów z pSS opracowanej w Korei zaobserwowano związek tych przeciwciał z różnymi objawami klinicznymi. Anty-Ro52 było najczęstszym autoprzeciwciałem i wiązało się z uszkodzeniem wątroby i mięśni.15 Ostatnie badanie przeprowadzone w populacji meksykańskiej w celu określenia częstości występowania pSS w SLE o niedawnym początku wykazało obecność anty-Ro/SSA jako predyktor nakładania się choroby, podczas gdy brak anty-Ro/SSA, anty-La/SSB i czynnika reumatoidalnego wiązał się z najmniejszym ryzykiem nakładania się choroby.16 Wreszcie, Szpital Uniwersytecki w Gandawie zaproponował badanie mające na celu określenie dystrybucji diagnostycznej związanej z serotypem anty-Ro/SSA lub anty-La/SSB u kolejnych pacjentów kierowanych do pracowni reumatologicznej. SLE był związany z anty-Ro60 dodatnim, a izolowany anty-La predysponował bardziej do pSS.17
Podjęliśmy to badanie, aby ocenić kliniczne, laboratoryjne i diagnostyczne powiązania tego ważnego podzbioru przeciwciał w szpitalu w Hiszpanii.
MetodyCentrum badawcze
Hospital de Jerez de la Frontera jest regionalnym ośrodkiem specjalistycznym zlokalizowanym w południowo-zachodniej Hiszpanii. Świadczy on specjalistyczne usługi kliniczne i dysponuje 550 łóżkami. Jego Oddział Immunologii analizuje rocznie około 5800 testów ANA i 1700 testów ENA metodą immunoblot w populacji liczącej 450 000 mieszkańców. Wśród personelu laboratoryjnego znajdują się biolog i immunolog, którzy wykonują specjalistyczne testy dla różnych oddziałów. Każdy praktykujący lekarz może zlecić badania przeciwciał przeciwjądrowych, ale są one zlecane głównie przez reumatologów, a następnie przez lekarzy podstawowej opieki zdrowotnej, gastroenterologów, internistów, nefrologów, pneumologów i hematologów.
Próbki
Komputerowy rejestr wyników laboratoryjnych jest dostępny od czerwca 2002 roku. Przeanalizowaliśmy retrospektywnie wszystkie kolejne próbki zlecające badanie ANA od czerwca 2002 do grudnia 2012 roku. Surowice z mianem co najmniej 1:160 w teście immunofluorescencyjnym na komórkach HEp-2 (Euroimmun, Niemcy) zostały uznane za pozytywne i wykonane przez jednego przeszkolonego obserwatora. Surowice z dodatnim wynikiem testu ANA dla tego rozcieńczenia miana były analizowane przy użyciu dostępnego w handlu testu ENA (INNO-LIA ANA, Fujirebio, Japonia). Zestaw ten zapewnia jakościowy test in vitro dla ludzkich autoprzeciwciał klasy IgG dla 13 różnych antygenów: RNP-70, RNP-A, RNP-C, Ro-52, Ro-60, La/SSB, Scl-70, CENP-B, histonów, Jo-1, Sm, białka rybosomalnego P i kompleksu U1-nRNP w surowicy lub osoczu. Ogólna czułość i swoistość wykrywania autoprzeciwciał za pomocą LIA była podobna lub wyższa w porównaniu do połączonych technik konwencjonalnych.18,19 Ten immunoblot ma 99,6% swoistość dla anty-La, podczas gdy anty-Ro60 ma 98,2%, a anty-Ro52 ma 98,3%.20
Dodatni wynik testu immunologicznego anty-Ro i/lub anty-La przy ujemnym teście ANA, ponieważ u pacjentów z wysokim klinicznym podejrzeniem choroby autoimmunologicznej test immunoblot ENA był wykonywany pomimo ujemnego testu ANA. Wreszcie, tylko pacjenci z więcej niż jedną pozytywną próbką surowicy dla anty-Ro/SSA lub anty-La/SSB zostali włączeni do badania.
Dane kliniczne i laboratoryjne zostały uzyskane przez dwóch przeszkolonych obserwatorów poprzez przegląd kart klinicznych lub skomputeryzowaną bazę danych laboratoryjnych.Zmienne
Zależne zmienne obejmowały dane demograficzne (wiek, płeć), kliniczne (diagnoza, charakterystyka choroby), laboratoryjne (hemoglobina, liczba leukocytów i płytek krwi, poziom hormonów tarczycy) lub immunologiczne (poziom dopełniacza, hipergammaglobulinemia, czynnik reumatoidalny).
Analiza statystyczna
Statystyki opisowe zostały użyte z częstotliwością i procentami dla zmiennych jakościowych oraz średnią, odchyleniem standardowym i zakresem dla zmiennych ilościowych. Asocjacje kliniczne pomiędzy różnymi zestawami pozytywnych kombinacji w stosunku do zmiennych klinicznych lub laboratoryjnych analizowano za pomocą tabel kontyngencji przy użyciu testu chi kwadrat lub dokładnego testu Fishera. We wszystkich przypadkach poziom alfa został ustalony na 0,01 jako korekta dla wielokrotnych porównań. Siła związku została przedstawiona jako iloraz szans i jego 99% przedział ufności. Przeprowadzono analizę skupień zmiennych z wykorzystaniem średnich powiązań między grupami, a jako miary interwałowej użyto kwadratu odległości euklidesowej. Analizy przeprowadzono przy użyciu programu SPSS 16.0 (SPSS Inc., Chicago, IL).
Wyniki
Do Zakładu Immunologii skierowano 41 102 próbki surowicy w celu wykrycia ANA. 12 124 próbki były dodatnie od 2970 pacjentów. Do badania włączono 322 pacjentów z więcej niż jedną dodatnią próbką surowicy dla przeciwciał anty-Ro52 i/lub anty-Ro60 i/lub anty-La o rozcieńczeniu miana >160. Kobiety stanowiły 90,4% badanej próby. Wiek badanych mieścił się w przedziale od 10 do 84 lat, średnia 44,4 roku, odchylenie standardowe 15,7 roku. Niektóre wyizolowane surowice były pozytywne dla testu immunoblot ENA z negatywnym testem ANA. Ale 322 pacjentów wykazało wszystkie lub większość surowic pozytywnych dla testu ANA, a wzór surowic dla każdego pacjenta był praktycznie identyczny. W naszym badaniu nie znaleziono pacjenta z więcej niż jedną surowicą negatywną dla IIF.
Główne dane kliniczne i laboratoryjne pacjentów z dodatnimi próbkami dla anty-Ro52 i/lub anty-Ro60 i/lub anty-La (322 przypadki) są przedstawione w Tabeli 1. Specyficzność różnych antygenów u tych pacjentów przedstawiono w Tabeli 2. Najczęściej stwierdzano obecność anty-Ro52 u 269 chorych (83,5%), następnie anty-Ro60 u 205 chorych (63,7%) i anty-La u 155 chorych (48,1%).
Tabela 3 przedstawia różne asocjacje pomiędzy kombinacją przeciwciał anty-Ro52/anty-Ro60/anty-La a rozpoznaniem, wynikami klinicznymi lub laboratoryjnymi. Tabela 4 pokazuje istotne związki między dodatnim wynikiem testu na obecność krążących przeciwciał anty-Ro52, anty-Ro60 i anty-La. Ze względu na ściśle określony poziom istotności, niektóre interesujące asocjacje nie zostały przedstawione, np. grupa anty-Ro52+ ze wzorem cytoplazmatycznym (OR 3,72, 99% CI: 0,9-16, p wartość 0,04) oraz grupa anty-Ro60+ z podostrym toczniem skórnym (SCLE) (OR 7,0, 99% CI: 0,9-55,3, p: 0,023).
Zastosowując analizę skupień, można wyodrębnić cztery grupy autoprzeciwciał. Klaster 1 obejmuje przeciwciała przeciwko SmB, SmD, RNP,70, RNP-A i RNP-C. Klaster 2 jest tworzony dla przeciwciał przeciwko Scl-70, Ribosomal P, Jo1 i centromerom. Skupisko 3 jest tworzone dla przeciwciał przeciwko Ro60 i SSB. Klaster 4 stanowiły przeciwciała przeciwko Ro52 (ryc. 1).
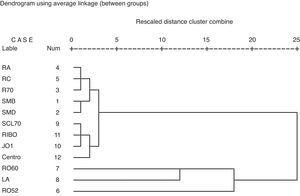
Analiza skupisk w celu identyfikacji skupisk przeciwciał w naszej próbie pacjentów.
Dyskusja
Reumatolodzy ustalili znaczenie klinicznych i serologicznych wyników w klasyfikacji wielu chorób autoimmunologicznych. Pojawiły się pewne wątpliwości dotyczące znaczenia krytycznej oceny testów specjalistycznych w opiece klinicznej. Wydaje się, że zlecenie wielu testów może prowadzić do uzyskania wielu wyników laboratoryjnych, które muszą być starannie oceniane w kontekście wyników klinicznych.17,21
W naszym badaniu opisujemy kliniczne, diagnostyczne i immunologiczne związki z wszystkimi kilkoma możliwymi kombinacjami przeciwciał anty-Ro52, anty-Ro60 i anty-La, stwierdzonymi w dużej kohorcie pacjentów z jednego ośrodka w Hiszpanii przez 10 lat. W sumie 322 pacjentów prezentowało więcej niż jedną dodatnią wartość tych przeciwciał, a najczęściej występującymi chorobami były SLE i pSS, głównie związane z profilem immunologicznym anty-Ro52+/anty-Ro60+/anty-La- i anty-Ro52+/anty-Ro60+/anty-La+, odpowiednio.
Nasza ścisła definicja istotności statystycznej mogła sprawić, że niektóre stowarzyszenia zostały utracone, ale jesteśmy pewni, że opisane stowarzyszenia mogą być bardziej solidne. Kliniczne i praktyczne znaczenie tych skojarzeń może być szczególnie interesujące dla izolowanych anty-Ro52 (anty-Ro52+/anti-Ro60-/anti-La-). Ta podgrupa autoprzeciwciał ma niezależne asocjacje kliniczne i immunologiczne, dane potwierdzone w naszej analizie skupień.22,23 Dodatnie izolowane przeciwciała anty-Ro52 były związane z twardziną układową, szczególnie u osób z zespołem CREST, i zapaleniem skórno-mięśniowym (OR 11,65, 99% CI: 1,28-105,79, p: 0,018). Inne asocjacje obserwowano głównie z niektórymi wynikami badań laboratoryjnych, takimi jak anty-Jo-1 (OR 3,45, 99% CI: 1,12-10,59, p: 0,03), anty-centromerowe (OR 2,66, 99% CI: 1,04-2,80, p: 0,03) lub określone wzory immunofluorescencji, takie jak wzór centromerowy, cytoplazmatyczny i nukleolarny. Ponadto, porównując izolowaną grupę z dodatnią reaktywnością anty-Ro52+ (anty-Ro52+/anty-Ro60-/anty-La-) z dodatnią reaktywnością potrójną (anty-Ro52+/anty-Ro60+/anty-La+), stwierdzone w jednej grupie asocjacje kliniczne, laboratoryjne i diagnostyczne były odwrotne w drugiej. I tak, podzbiór immunologiczny anty-Ro52+/anty-Ro60+/anty-La+ był dodatnio związany z kserostomią i drobnoplamistością, a ujemnie z twardziną układową (OR 0,22, 99% CI: 0,05-1,00, p: 0,026). Podkreśla to diagnostyczną wartość kliniczną tej kombinacji. W odniesieniu do dodatniego wyniku testu dla grupy anty-Ro60+, głównie związanego z anty-La- (anty-Ro52+/anti-Ro60+/anti-La- i anty-Ro52-/anti-Ro60+/anti-La-), był bardzo wskazujący dla SLE.
Nasze wyniki są podobne do wcześniejszych doniesień.6,22-25 Obecność krążących przeciwciał anty-Ro52, anty-Ro60 i anty-La dodatnich predysponowała do kserostomii i kseroftalmii (kserostomia w grupie anty-Ro60 OR 1,75, 99% CI: 1,10-2,79, p: 0,012). Te dane kliniczne poparte są licznymi badaniami nad pSS.6-9,11,17,24 Dodatnie anty-Ro52 z ujemnymi anty-Ro60 i anty-La wykazywały negatywny związek z fotowrażliwością, jednak we wcześniejszych badaniach pacjenci z anty-Ro52+ mieli większą częstość zajęcia skóry.17,26 Co więcej, ta kombinacja immunologiczna (anty-Ro52+/anty-Ro60-/anty-La-) była również odwrotnie związana z kserostomią i kseroftalmią. Jednak w poprzednich badaniach izolowane dodatnie anty-Ro52 było ściśle związane z głównymi klinicznymi, histopatologicznymi i immunologicznymi cechami pSS.27 Izolowane dodatnie anty-Ro60 lub anty-Ro60+ w połączeniu z anty-Ro52+ zwiększało prawdopodobieństwo SLE lub nakładania się SLE/SS, jak opisano w kilku pracach,11,17,28 ale także w naszej kohorcie było silnie związane z owrzodzeniami jamy ustnej i zapaleniem stawów. Reaktywność anty-La była silnie związana z pSS i jego głównymi objawami klinicznymi (kserostomia i kseroftalmia), podobnie jak w wielu innych badaniach w różnych populacjach.11,17,26
Większość wcześniejszych badań nad przydatnością tych przeciwciał przeprowadzono na próbkach pochodzących od pacjentów z rozpoznaną chorobą autoimmunologiczną, zwłaszcza SLE i SS. Niewiele jest jednak badań opisujących związek diagnostyczny przeciwciał anty-Ro i anty-La zidentyfikowanych w kolejnych próbkach.17
Oprócz diagnostyki, określiliśmy przydatność profili immunologicznych z anty-Ro52 i/lub anty-Ro60 i/lub anty-La w przewidywaniu danych klinicznych i laboratoryjnych w kolejnych próbkach pacjentów, które są zamawiane do wszystkich oddziałów szpitala i podstawowej opieki zdrowotnej. Przejrzeliśmy wszystkie próbki każdego pacjenta w tym okresie i zarejestrowaliśmy częściej występującą kombinację reaktywności anty-Ro52, anty-Ro60 i anty-La. Wybrany punkt odcięcia dla dodatniej reaktywności >160 zwiększa wiarygodność badania, ponieważ dodatni wynik testu ANA oraz oznaczenia anty-Ro/SSA i anty-La/SSB mogą być wykryte odpowiednio u 25-30% i 1,6% zdrowych osób. Częstość ich występowania jest większa wraz z wiekiem, a ich dodatni wynik bez odpowiednich danych klinicznych może być mylący.29
W naszym badaniu wykazaliśmy zatem, że profil immunologiczny może nas naprowadzić na pewne rozpoznanie lub rozwój objawów chorobowych. Ma to większe znaczenie w początkach chorób autoimmunologicznych, ponieważ krążące przeciwciała mogą być obecne na kilka lat przed rozpoznaniem choroby i mogą wskazywać na ciężkość jej manifestacji.17,30
Pewnymi ograniczeniami, nieodłącznie związanymi z tymi badaniami, są retrospektywne oceny kliniczne kart klinicznych i możliwe uprzedzenia diagnostyczne lekarzy prowadzących, którzy widzą tych pacjentów i zlecają specjalistyczne badania laboratoryjne. Wielu z naszych pacjentów z dodatnim wynikiem testu ANA uzyskało wynik ujemny w teście immunoblot ENA. Może to być związane z rodzajem opracowanego testu immunologicznego. W przypadkach o dużym podejrzeniu klinicznym zaleca się oznaczanie swoistych przeciwciał.11
Ujawnienia etyczneOchrona ludzi i zwierzątAutorzy oświadczają, że w tym badaniu nie przeprowadzano eksperymentów na ludziach ani zwierzętach.Poufność danychAutorzy oświadczają, że postępowali zgodnie z protokołami miejsca pracy dotyczącymi publikacji danych pacjentów.Prawo do prywatności i świadoma zgodaAutorzy oświadczają, że w tym artykule nie pojawiają się dane pacjentów.Konflikt interesówAutorzy nie zgłaszają konfliktu interesów.