Kwas cynamonowy Właściwości chemiczne, zastosowania, produkcja
Właściwości chemiczne
Kwas cynamonowy występuje w formie cis i trans. bardziej stabilnym izomerem jest izomer trans, który występuje naturalnie i jest zwykłym produktem handlowym. Występuje jako białe monokliniczne pryzmaty z lekkim cynamonowym aromatem. Jest rozpuszczalny w etanolu, metanolu, eterze naftowym i chloroformie; jest łatwo rozpuszczalny w benzenie, eterze, acetonie, kwasie octowym, dwusiarczku węgla i olejach, ale nierozpuszczalny w wodzie.
Kwas cynamonowy został po raz pierwszy wyizolowany jako kryształy z olejku cynamonowego przez Trommsdorfa w 1780 roku. Uważał on, że jest to kwas benzoesowy. Dumas i Peligot zidentyfikowali go w 1835 r., a w 1856 r. Bertagniniemu udało się go zsyntetyzować z benzaldehydu i chlorku acetylu.
Kwas cynamonowy ulega reakcjom typowym dla grupy karboksylowej i podwójnego wiązania olefinowego. Grupa karboksylowa może być zestryfikowana tworząc cynamoniany, z których niektóre są ważnymi środkami aromatyzującymi i zapachowymi. W reakcji z nieorganicznymi chlorkami kwasowymi, takimi jak chlorek tionylu lub chlorek fosforu, kwas cynamonowy daje chlorek cynamonowy. Po podgrzaniu kwas cynamonowy tworzy styren i dwutlenek węgla. Z utleniaczami lub po podgrzaniu z alkaliami, podwójne wiązanie olefinowe rozszczepia się dając benzaldehyd.
Właściwości fizyczne i chemiczne
Kwas cynamonowy, znany również jako octan benzalu, kwas 3-fenylo-2-propenowy, należy do rodzaju nienasyconych kwasów aromatycznych o lekkim zapachu cynamonu. Występuje w balsamie, olejku cynamonowym i liściach koki w postaci wolnej lub estrowej. Ze względu na obecność wiązania podwójnego, kwas cynamonowy posiada izomery trans- / cis-dwa, przy czym forma cis zawiera dodatkowo trzy rodzaje jednorodnych polikryształów. Zarówno trans-form i cis-form są w obecności natury. Forma trans występuje w obecności olejków eterycznych, w tym storax, olejku cynamonowego, balsamu peruwiańskiego, olejku bazyliowego i liści kakaowca. Forma cis występuje w olejku galangalu z Malacca, przy czym forma trans jest bardziej stabilna niż forma cis. Produkty dostępne w handlu występują głównie w formie trans. Jego względna masa cząsteczkowa wynosi 148,17. Pierwsza forma krystaliczna formy cis jest nazywana kwasem alokinnamonowym, a związek wytrącający się z wody jest monokliniczny. Jest bezbarwny do białych pryzmatycznych kryształów o gęstości względnej 1,284 (4 ℃), temperatura topnienia 42 ℃, temperatura wrzenia 265 ℃ (rozkład ) i 125 ℃ (2,533 × 103Pa); jest słabo rozpuszczalny w wodzie (25 ℃, gdy 0,937), ale łatwo rozpuszczalny w alkoholu, eterze i octanie etylu.Drugi polimorf nazywa się kwas alfa-izo-cynamonowy ze związkiem wytrąconym z ligroiny jest monokliniczny kryształ. Jest to bezbarwne do białych kryształów pryzmatycznych z mp jest 58 ℃ i temperatury wrzenia 265 ℃. Jest rozpuszczalny w etanolu, kwasie octowym, chloroformie i acetonie i łatwo rozpuszczalny w eterze. Trzeci polimorf jest nazywany beta-izo-cynamonowego kwasu; pojawia się jako monokliniczne bezbarwne do białych kryształów pryzmatycznych z mp jest 68 ℃. Jest rozpuszczalny w alkoholu, eterze, kwasie octowym, chloroformie i acetonie. Trans-izomer wytrąca się z rozcieńczonego etanolu należy do monoklinicznych kryształów i pojawia się jako białe do jasnożółtych kryształów pryzmatycznych o gęstości względnej 1,2475 (4 ℃), temperatura topnienia wynosi 133 ℃, a temperatura wrzenia wynosi 300 ℃. Jest bardzo słabo rozpuszczalny w wodzie (25 ℃: 0,1; 98 ℃: 0,588), rozpuszczalny w etanolu (25 ℃: 23), chloroform (15 ℃: 5,9), łatwo rozpuszczalny w benzenie, eterze, acetonie, kwasie octowym i disiarczku węgla. Podczas destylacji w temperaturze 140 ℃ ulega dekarboksylacji, stając się styrenem (Styrax BP). W wyniku utleniania powstaje kwas benzoesowy. Zarówno izomery cis- i trans- mają kwiatowo-miodowy aromat ze słodkim i pikantnym smakiem. LD50 w jamie ustnej szczura: 2500 mg/kg.
Rola i cel
Kwas cynamonowy jest ważnym rodzajem organicznego surowca syntetycznego. Stosowany jest głównie do syntezy cynamonianu metylu, cynamonianu etylu i estru benzylowego kwasu cynamonowego. Jest on szeroko stosowany w przemyśle perfumeryjnym i farmaceutycznym. W medycynie, to był kiedykolwiek używany jako środek odstraszający owady.
Kwas cynamonowy był używany jako przyprawy do przygotowania wiśni, moreli, miodu i cynamonu aromatów i smaków, może być również stosowany jako materiał wyjściowy ester kwasu cynamonowego. GB2760-1996 naszego kraju przewiduje, że kwas cynamonowy jest dopuszczalną przyprawą jadalną; ponadto może być również stosowany jako surowiec do produkcji światłoczułej żywicy z serii kwasu poliwinylowego cynamonowego; może być również stosowany jako surowiec do syntezy estrów metylowych, etylowych i benzylowych. Estry te, stosowane jako substancje zapachowe, mogą być stosowane do produkcji kosmetyków i mydła, mogą być również stosowane jako miejscowe środki znieczulające, środki hemostatyczne i surowce farmaceutyczne (kwas mlekowy, prenylamina i baklofen itp.); kwas cynamonowy może być również stosowany jako regulatory wzrostu roślin i surowce do produkcji pestycydów; środki antykorozyjne do owoców i warzyw; surowiec do produkcji środków ultrafioletowych i żywica światłoczuła do produkcji kosmetycznych filtrów przeciwsłonecznych. Kwas cynamonowy może być również stosowany jako standard w organicznej analizie śladowej i określaniu podwójnego wiązania, określaniu separacji uranu i wanadu i toru.
Zastosowanie
Kwas cynamonowy jest ważnym półproduktem w przygotowaniu jego estrów, które są stosowane jako substancje zapachowe, w farmaceutykach oraz w enzymatycznej produkcji l-fenyloalaniny, materiału wyjściowego do peptydowych substancji słodzących. Cynamonian sodu jest znanym inhibitorem korozji. Kwas cynamonowy jest również stosowany jako rozjaśniacz w bezcyjankowych kąpielach galwanicznych, jako inhibitor korozji podczas usuwania zgorzeliny z cynku i w puszkach aerozolowych, jako niskotoksyczny stabilizator termiczny poli(chlorku winylu), jako środek sieciujący w kopolimerze tereftalanu dimetylu z glikolem etylenowym i w poliuretanach, jako środek ognioodporny w polikaprolaktamie, w odpornych na pranie klejach poliuretanowych do włókien poliestrowych oraz do poprawy stabilności przechowywania powłok z żywicy alkidowej modyfikowanej olejem suszarniczym.
Przygotowanie
Kwas cynamonowy jest również wytwarzany przez kondensację Knoevenagela benzaldehydu z kwasem malonowym w obecności słabo zasadowych katalizatorów, takich jak amoniak i aminy.
Refluksować razem 10ml benzaldehydu z 10gm kwasu malonowego i 40ml 8% etanolowego roztworu amoniaku umieszczonego w 100ml kolbie okrągłodennej wyposażonej w chłodnicę zwrotną na łaźni wodnej do uzyskania klarownego roztworu (około 8-10 godzin). Ustawić zestaw do destylacji w dół i oddestylować nadmiar alkoholu. Kontynuować ogrzewanie pozostałej części oleistej do momentu ustania wydzielania się dwutlenku węgla. Rozpuścić pozostałość w 20 ml wody, schłodzić i dodać rozcieńczony kwas solny do uzyskania kwaśnego odczynu. Zebrać wytrącający się nienasycony kwas na lejku Buchnera, przemyć zimną wodą. Skrystalizować ponownie w gorącej wodzie i zebrać kryształy kwasu cynamonowego, m.p. 132°C.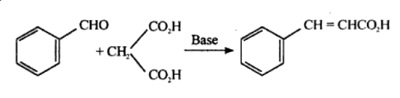
Synteza kwasu cynamonowego z benzaldehydu
Analiza zawartości
Dokładnie odważyć 500 mg próbki, którą uprzednio suszono przez 3 godziny w suszarce wypełnionej żelem krzemionkowym; dodać 0,1mol/L wodoru.
Toksyczność
GRAS (FEMA).
Ostra doustna LD50 u szczurów wynosi 2,5 g/kg, a ostra skórna LD50 u królików przekracza 5 g/kg. Kwas cynamonowy stosowany w stanie czystym na nienaruszoną lub otartą skórę królika przez 24 godziny był lekko drażniący; 4% roztwór w petrolatum nie powodował uczuleń u ludzi.
Zastrzeżone zastosowanie
FEMA (mg/kg): Soft drinks 31; Cold drink 40; Confectionery 30; Bakery 36; Gum 10.
Przyjmij umiarkowaną wartość jako wartość graniczną (FDA§172.515, 2000).
Metoda produkcji
Komercyjna synteza kwasu cynamonowego prawie zawsze prowadzi do izomeru trans.
Reakcja Perkina jest najstarszą znaną metodą komercyjnej produkcji kwasu cynamonowego. W tej reakcji benzaldehyd jest kondensowany z bezwodnikiem octowym w obecności octanu sodu jako katalizatora.
Chlorek benzalu reaguje z octanem alkalicznym w środowisku alkalicznym, dając wysoką wydajność kwasu cynamonowego. Kwas cynamonowy można otrzymać w tej reakcji w obecności amin, takich jak pirydyna, z wydajnością powyżej 80 %.
Można go również otrzymać poprzez: mieszanie benzoiloacetonu, węglanu sodu i wybielacza, wytwarzając kwas cynamonowy sodu, a następnie przetwarzanie siarczanem.
Opis
Kwas cynamonowy jest białym krystalicznym kwasem organicznym, który jest słabo rozpuszczalny w wodzie.
Jest otrzymywany z olejku cynamonowego lub z balsamów takich jak storax. Występuje również w maśle shea i jest najlepszym wskaźnikiem jego historii środowiskowej i warunków poekstrakcyjnych. Może być również wytwarzany syntetycznie.
Kwas cynamonowy jest stosowany w aromatach, syntetycznym indygo i niektórych farmaceutykach, choć jego głównym zastosowaniem jest produkcja estrów metylowych, etylowych i benzylowych dla przemysłu perfumeryjnego. Kwas cynamonowy ma zapach podobny do miodu; on i jego bardziej lotny ester etylowy (cynamonian etylu) są składnikami aromatu w olejku eterycznym cynamonu, w którym powiązany z nim aldehyd cynamonowy jest głównym składnikiem. Kwas cynamonowy jest również częścią biosyntetycznego szlaku shikimatowego i fenylopropanoidowego. Jego biosynteza odbywa się w wyniku działania enzymu amoniakalnej liazy fenyloalaniny (PAL) na fenyloalaninę.
Kwas cynamonowy jest łatwo rozpuszczalny w benzenie, eterze dietylowym, acetonie, natomiast jest nierozpuszczalny w heksanie.
Kwas cynamonowy jest również rodzajem autoinhibitora produkowanego przez zarodniki grzybów, aby zapobiec kiełkowaniu.
Właściwości chemiczne
Kwas cynamonowy jest prawie bezwonny z palącym smakiem, a następnie staje się słodki i przypomina morelę. ystępowanie Forma trans została znaleziona wśród składników olejków eterycznych bazylii, cynamonu chińskiego, Melaleuca bracteata, Alpinia galanga. Podaje się, że występuje w balsamie peruwiańskim, azjatyckim i amerykańskim storaksie oraz liściach kakaowca. Znaleźć go można również w owocach truskawki, piwie, koniaku, owocach gwiaździstych (Averrhoa carambola L) oraz w liściach kakaowca. Forma cis- występuje w olejku z Alpinia malacensis.
Zastosowanie
zapach & środek aromatyzujący, przeciwcukrzycowy
Zastosowanie
kwas cynamonowy ma zdolności przeciwsłoneczne. Niektórzy producenci stosują go zamiast PABA ze względu na mniejszą częstość występowania reakcji alergicznych i fototoksycznych. Kwas cynamonowy występuje w liściach cynamonu i kakaowca, a także jest olejkiem eterycznym niektórych grzybów. Może powodować alergiczne wysypki skórne.
Zastosowanie
Kwas cynamonowy jest środkiem aromatyzującym, który składa się z krystalicznych łusek, koloru białego, o zapachu przypominającym miód i kwiaty. jest słabo rozpuszczalny w wodzie, rozpuszczalny w alkoholu, chloroformie, kwasie octowym, acetonie, benzenie i większości olejów, oraz w solach alkalicznych rozpuszczalnych w wodzie. jest otrzymywany w drodze syntezy chemicznej. jest również określany jako kwas 3-fenylopropenowy.
Definicja
ChEBI: Kwas monokarboksylowy, który składa się z kwasu akrylowego opatrzonego podstawnikiem fenylowym w pozycji 3. Występuje w Cinnamomum cassia.
Przygotowanie
Istnieją dwa izomery, trans- i cis-; izomer trans jest interesujący do stosowania w aromatyzacji; oprócz ekstrakcji ze źródeł naturalnych (storax), może być przygotowany w następujący sposób: (1) z benzaldehydu, bezwodnego octanu sodu i bezwodnika octowego w obecności pirydyny (reakcja Perkina); (2) z benzaldehydu i octanu etylu (kondensacja Claisena); (3) z benzaldehydu i chlorku acetylenu; (4) przez utlenianie benzylidenoacetonu podchlorynem sodu.
Podstawa(y)
Journal of the American Chemical Society, 75, s. 1068, 1953 DOI: 10.1021/ja01101a016
The Journal of Organic Chemistry, 59, s. 710, 1994 DOI: 10.1021/jo00083a006
Profil bezpieczeństwa
Trucizna drogą dożylną i dootrzewnową. Umiarkowanie toksyczny po połknięciu. Działa drażniąco na skórę. Łatwopalna ciecz. Po podgrzaniu do rozkładu wydziela ostry dym i dymy.
Synteza chemiczna
Rainer Ludwig Claisen (1851-1930), niemiecki chemik, w 1890 r. po raz pierwszy opisał syntezę cynamonianów poprzez reakcję aldehydów aromatycznych z estrami. Reakcja ta znana jest jako kondensacja Claisena.
Metody oczyszczania
Kwas krystalizuje się z *benzenu, CCl4, gorącej wody, wody/EtOH (3:1) lub 20% wodnego EtOH. Suszyć w temperaturze 60o w vacuo. Jest lotny z parą wodną.