Um sistema refere-se a qualquer parte do universo em estudo.
Se estiver a realizar uma experiência num copo, então o sistema que está a estudar está no copo.
O sistema está sujeito a factores circundantes como a temperatura e pressão do ar.
Termodinâmica envolve o estudo da troca de energia térmica entre um sistema e o seu ambiente.
Existem três tipos de sistemas termodinâmicos. Com base na possível transferência de calor e matéria, eles são classificados como sistemas abertos, fechados ou isolados.
Tipos de Sistemas Termodinâmicos
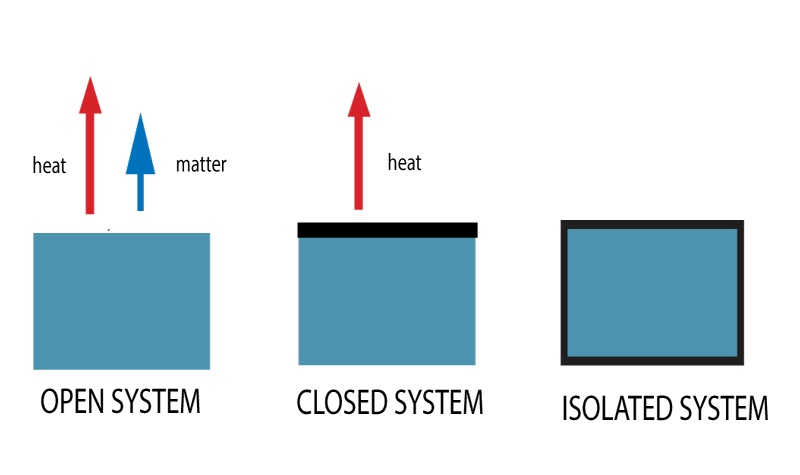
Sistemas Abertos
 p>>p>Talvez já tenha ouvido falar de sistemas abertos e sistemas fechados. Um sistema aberto é aquele que permite livremente a transferência de energia e matéria num sistema.
p>>p>Talvez já tenha ouvido falar de sistemas abertos e sistemas fechados. Um sistema aberto é aquele que permite livremente a transferência de energia e matéria num sistema.
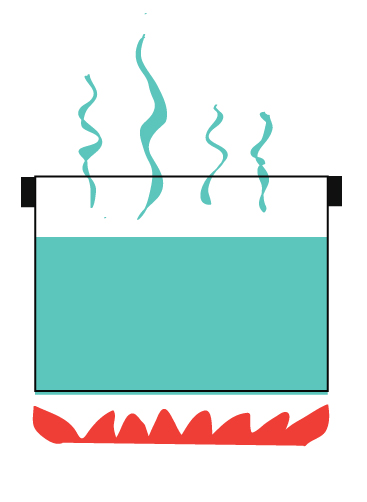
Por exemplo, água a ferver sem tampa.
Calor a escapar para o ar.
Vapor (que é matéria) a escapar para o ar.
Sistemas fechados
 br>Um sistema fechado, por outro lado, não permite a troca de matéria mas permite a transferência de energia.
br>Um sistema fechado, por outro lado, não permite a troca de matéria mas permite a transferência de energia.
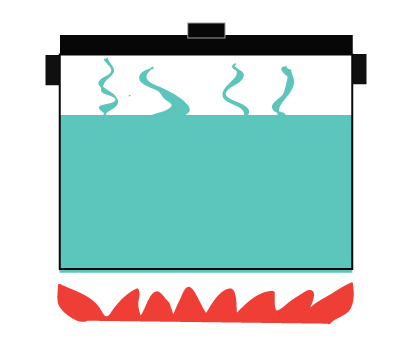
Permite transferir calor do fogão para a água
O calor também é transferido para o ambiente
Vapor não é permitido escapar
Exemplo de um sistema fechado – uma panela de pressão.
Nb: If a system is 100% closed, it is in danger of exploding. That's why a pressure cooker should be designed with safety mechanisms to prevent the system from over-pressurzing by allowing steam to escape when needed.
Sistemas isolados
Este sistema é completamente selado.
Nada matéria nem calor pode transferir para ou do ambiente circundante.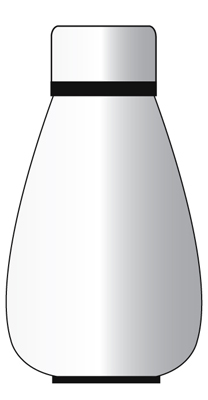 Exemplo – Um frasco térmico.
Exemplo – Um frasco térmico.
O objectivo de um frasco térmico é manter a sua comida quente.
Um frasco térmico pode ser considerado um sistema isolado mas apenas por um curto período de tempo.
Impede que tanto o calor como a matéria sejam transferidos para o ambiente.
Ultimamente, o calor no frasco térmico escapará para o ambiente e o conteúdo dentro do frasco será arrefecido.