Acido cinnamico Proprietà chimiche, usi, produzione
Proprietà chimiche
L’acido cinnamico esiste nelle forme cis e trans. L’isomero più stabile è quello trans, che si presenta naturalmente ed è il prodotto commerciale abituale. Si presenta come prismi monoclinici bianchi con un leggero aroma di cannella. È solubile in etanolo, metanolo, etere di petrolio e cloroformio; è facilmente solubile in benzene, etere, acetone, acido acetico, disolfuro di carbonio e oli, ma insolubile in acqua.
L’acido cinnamico fu isolato per la prima volta come cristalli dall’olio di cannella da Trommsdorf nel 1780. Egli pensava che si trattasse di acido benzoico. Dumas e Peligot lo identificarono nel 1835, e nel 1856 Bertagnini riuscì a sintetizzarlo da benzaldeide e cloruro di acetile.
L’acido cinnamico subisce reazioni tipiche di un gruppo carbossilico e un doppio legame olefinico. Il gruppo carbossilico può essere esterificato per formare cinnamati, alcuni dei quali sono importanti aromi e fragranze. Quando reagisce con cloruri acidi inorganici, come il cloruro di tionile o i cloruri di fosforo, l’acido cinnamico dà cloruro di cinnamoile. Se riscaldato, l’acido cinnamico forma stirene e biossido di carbonio. Con agenti ossidanti o se riscaldato con alcali, il doppio legame olefinico si scinde per dare benzaldeide.
Proprietà fisiche e chimiche
L’acido cinnamico, conosciuto anche come acetato di benzal, acido 3-fenil-2-propenoico, appartiene ad un tipo di acido aromatico insaturo con un leggero odore di cannella. Si presenta nel balsamo, nell’olio di cannella e nella foglia di coca in forma libera o sotto forma di estere. A causa della presenza di un doppio legame, l’acido cinnamico ha trans-/ cis-due isomeri con la forma cis che contiene tre tipi di policristalli omogenei in più. Sia la forma trans che la forma cis sono presenti in natura. La forma trans esiste in presenza di oli essenziali tra cui storace, olio di cannella, balsamo peruviano, olio di basilico e foglie di cacao. La forma cis esiste nell’olio di galanga di Malacca e la forma trans è più stabile della forma cis. I prodotti disponibili in commercio sono per lo più nella forma trans. Ha una massa molecolare relativa di 148,17. La prima forma cristallina della forma cis è chiamata acido allocinnamico e il composto precipitato dall’acqua è monoclino. È incolore ai cristalli prismatici bianchi con la densità relativa che è 1.284 (4 ℃), il punto di fusione che è 42 ℃, il punto di ebollizione 265 ℃ (decomposizione) e 125 ℃ (2.533 × 103Pa); è leggermente solubile in acqua (25 ℃ quando 0.937) ma facilmente solubile in alcool, etere ed etil acetato.Il secondo polimorfo è denominato acido alfa-iso-cinnamico con il composto precipitato da ligroin che è il cristallo monoclino. È incolore ai cristalli prismatici bianchi con il mp che è 58 ℃ ed il punto di ebollizione che è 265 ℃. È solubile in etanolo, acido acetico, cloroformio e acetone e facilmente solubile in etere. Il terzo polimorfo è chiamato acido beta-iso-cinnamico; appare come cristalli prismatici monoclinici incolori o bianchi con un mp di 68 ℃. È solubile in alcool, etere, acido acetico, cloroformio e acetone. Il trans-isomero precipitato da etanolo diluito appartiene al cristallo monoclino e appare come bianco a cristalli prismatici giallo pallido con la densità relativa che è 1.2475 (4 ℃), il punto di fusione che è 133 ℃ ed il punto di ebollizione che è 300 ℃. È molto leggermente solubile in acqua (25 ℃: 0,1; 98 ℃: 0,588), solubile in etanolo (25 ℃: 23), cloroformio (15 ℃: 5,9), facilmente solubile in benzene, etere, acetone, acido acetico e disolfuro di carbonio. Quando viene distillato a 140 ℃, subisce la decarbossilazione per diventare stirene (Styrax BP). All’ossidazione, genera acido benzoico. Entrambi gli isomeri cis e trans hanno un aroma di miele di fiori con un sapore dolce e speziato. Rat-Oral LD50: 2500 mg/kg.
Ruolo e scopo
L’acido cinnamico è un tipo importante di materia prima sintetica organica. È usato principalmente per la sintesi del cinnamato di metile, del cinnamato di etile e dell’estere benzilico dell’acido cinnamico. È ampiamente usato nell’industria dei profumi e nell’industria farmaceutica. In medicina, è stato sempre usato come repellente per gli insetti.
L’acido cinnamico è stato usato come spezie per la preparazione di aromi e sapori di ciliegia, albicocca, miele e cannella; può anche essere usato come materiale di partenza dell’estere di acido cinnamico. Il GB2760-1996 del nostro paese ha previsto che l’acido cinnamico è spezie commestibili ammissibili; inoltre, può anche essere usato come materia prima della resina fotosensibile serie di acido polivinil cinnamico; può anche essere usato come materia prima per la sintesi di esteri metilici, etilici e benzilici. Questi esteri, essendo usati come fragranze, possono essere applicati a cosmetici e saponi, può anche essere usato come anestetico locale, agenti emostatici e materie prime farmaceutiche (acido lattico Prenylamine e baclofen, ecc.); l’acido cinnamico può anche essere usato come regolatori di crescita delle piante e materie prime di pesticidi; agenti anticorrosivi di frutta e verdura; materia prima di agente ultravioletto e resina fotosensibile per la protezione solare cosmetica. L’acido cinnamico può anche essere usato come standard per l’analisi delle tracce organiche e la determinazione del doppio legame, la determinazione dell’uranio e del vanadio e la separazione del torio.
Usi
L’acido cinnamico è un importante intermedio nella preparazione dei suoi esteri, che sono usati come fragranze, per i prodotti farmaceutici, e per la produzione enzimatica di l-fenilalanina, il materiale di partenza per i dolcificanti peptidici. Il cinnamato di sodio è un noto inibitore di corrosione. L’acido cinnamico è anche usato come sbiancante nei bagni galvanici di zinco senza cianuro, come inibitore di corrosione durante la rimozione delle incrostazioni dallo zinco e nelle bombolette spray, come stabilizzatore termico a bassa tossicità per il poli(cloruro di vinile), come agente reticolante per il copolimero dimetiltereftalato – etilenglicole e poliuretani, come agente ignifugo per il policaprolattame, negli adesivi poliuretanici resistenti al bucato per le fibre di poliestere, e per il miglioramento della stabilità di stoccaggio dei rivestimenti in resina alchidica modificati con olio essiccante.
Preparazione
L’acido cinnamico è anche prodotto dalla condensazione di Knoevenagel della benzaldeide con l’acido malonico in presenza di catalizzatori debolmente basici, come l’ammoniaca e le ammine.
Refluire insieme 10ml di benzaldeide con 10gm di acido malonico e 40ml di soluzione etanolica di ammoniaca all’8% posta in un pallone a fondo rotondo da 100ml dotato di un condensatore a riflusso a bagnomaria fino ad ottenere una soluzione chiara (circa 8-10 ore). Impostare il gruppo per la distillazione verso il basso e distillare l’alcool in eccesso. Continuare a riscaldare la parte oleosa residua fino alla cessazione dell’evoluzione dell’anidride carbonica. Sciogliere il residuo in 20 ml di acqua, raffreddare e aggiungere acido cloridrico diluito fino a quando non diventa acido. Raccogliere l’acido insaturo precipitato in un imbuto di buchner, lavare con acqua fredda. Ricristallizzare da acqua calda e raccogliere i cristalli di acido cinnamico, m.p 132°C.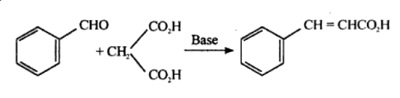
Sintesi dell’acido cinnamico dalla benzaldeide
Analisi del contenuto
Pesare accuratamente 500 mg di campione che sono stati precedentemente essiccati per 3 ore in essiccatore pieno di gel di silice; aggiungere 0,1mol/L di idrogeno.
Tossicità
GRAS (FEMA).
La DL50 acuta orale nei ratti è di 2,5 g/kg, e la DL50 acuta dermica nei conigli supera i 5 g/kg. L’acido cinnamico applicato puro sulla pelle intatta o abrasa del coniglio per 24 ore è stato leggermente irritante; una soluzione al 4% in petrolato non ha prodotto sensibilizzazione nell’uomo.
Uso limitato
FEMA (mg/kg): Bibite 31; Bevanda fredda 40; Pasticceria 30; Panetteria 36; Gomma 10.
Considerare moderato come limite (FDA§172.515, 2000).
Metodo di produzione
La sintesi commerciale dell’acido cinnamico risulta quasi sempre nell’isomero trans.
La reazione Perkin è il più antico metodo conosciuto per produrre commercialmente l’acido cinnamico. In questa reazione la benzaldeide viene condensata con l’anidride acetica in presenza di acetato di sodio come catalizzatore.
Il cloruro di benzal reagisce con l’acetato alcalino in un mezzo alcalino per dare un’alta resa di acido cinnamico. L’acido cinnamico può essere ottenuto da questa reazione in presenza di ammine come la piridina in una resa superiore all’80%.
Può anche essere preparato attraverso: miscelazione di benzoilacetone, carbonato di sodio e candeggina, generando acido cinnamico di sodio, seguito da lavorazione con solfato.
Descrizione
L’acido cinnamico è un acido organico bianco cristallino, leggermente solubile in acqua.
Si ottiene dall’olio di cannella, o da balsami come lo storace. Si trova anche nel burro di karité ed è la migliore indicazione della sua storia ambientale e delle condizioni post-estrazione. L’acido cinnamico è usato in aromi, indaco sintetico e alcuni prodotti farmaceutici, anche se il suo uso principale è nella produzione di esteri metilici, etilici e benzilici per l’industria dei profumi. L’acido cinnamico ha un odore simile al miele; esso e il suo estere etilico più volatile (etil cinnamato) sono componenti aromatici nell’olio essenziale di cannella, in cui la cinnamaldeide correlata è il costituente principale. L’acido cinnamico fa anche parte delle vie biosintetiche dello shikimate e dei fenilpropanoidi. La sua biosintesi viene effettuata dall’azione dell’enzima fenilalanina ammoniaca – liasi (PAL) sulla fenilalanina.
L’acido cinnamico è liberamente solubile in benzene, etere dietilico, acetone, ed è insolubile in esano.
L’acido cinnamico è anche un tipo di auto-inibitore prodotto da spore fungine per impedire la germinazione.
Proprietà chimiche
L’acido cinnamico è quasi inodore con un gusto bruciante, e poi diventa dolce e ricorda l’albicocca.
Eccursione
La forma trans è stata trovata tra i costituenti degli oli essenziali di basilico, cannella cinese, Melaleuca bracteata, Alpinia galanga. È stato riportato trovato nel balsamo del Perù, nello storace asiatico e americano e nelle foglie di cacao. Alsoreported trovato nel frutto della fragola, nella birra, nel cognac, nella carambola (Averrhoa carambola L) e nel nespolo. La forma cis- è presente nell’olio diAlpinia malacensis.
Usi
profumo & agente aromatizzante, antidiabetico
Usi
l’acido cinnamico ha capacità di protezione solare. Alcuni produttori lo usano per sostituire il PABA a causa della sua minore incidenza di reazioni allergiche e fototossiche. L’acido cinnamico si trova nelle foglie di cannella e nelle foglie di cacao, ed è un olio essenziale di alcuni funghi. Può causare eruzioni cutanee allergiche.
Usi
L’acido cinnamico è un agente aromatizzante che consiste in scaglie cristalline, di colore bianco, con un odore che ricorda il miele e i fiori. è leggermente solubile in acqua, solubile in alcool, cloroformio, acido acetico, acetone, benzene e la maggior parte degli oli, e sali alcalini solubili in acqua. è ottenuto per sintesi chimica. è anche chiamato acido 3-fenilpro-penoico.
Definizione
ChEBI: Un acido monocarbossilico che consiste in acido acrilico con un sostituente fenilico in posizione 3. Si trova nel Cinnamomum cassia.
Preparazione
Esistono due isomeri, trans- e cis-; l’isomero trans è di interesse per l’uso in aromi; oltre all’estrazione da fonti naturali (storace), può essere preparato come segue: (1) da benzaldeide, acetato di sodio anidro e anidride acetica in presenza di piridina (reazione di Perkin); (2) da benzaldeide e acetato di etile (condensazione di Claisen); (3) da benzaldeide e cloruro di acetilene; (4) per ossidazione di benzilidene acetone con ipoclorito di sodio.
Riferimenti sulla sintesi
Journal of the American Chemical Society, 75, p. 1068, 1953 DOI: 10.1021/ja01101a016
The Journal of Organic Chemistry, 59, p. 710, 1994 DOI: 10.1021/jo00083a006
Profilo di sicurezza
Veleno per via intravenosa e intraperitoneale. Moderatamente tossico per ingestione. Irritante per la pelle. Liquido combustibile. Se riscaldato fino alla decomposizione emette fumo acre e fumi.
Sintesi chimica
Rainer Ludwig Claisen (1851-1930), chimico tedesco, ha descritto per la prima volta nel 1890 la sintesi dei cinnamati facendo reagire aldeidi aromatiche con esteri. La reazione è nota come condensazione di Claisen.
Metodi di purificazione
Cristallizzare l’acido da *benzene, CCl4, acqua calda, acqua/EtOH (3:1), o EtOH acquoso al 20%. Asciugare a 60o in vacuo. È volatile a vapore.