
Bien, entonces — ¿qué es un átomo y qué tiene que ver con las moléculas?
Hablemos de lo más pequeño, y me refiero a lo más pequeño. Los átomos son los componentes básicos de todo lo que puedes ver a tu alrededor, e incluso de muchas cosas que no puedes ver, como el aire que respiras. Los átomos son tan pequeños que hay millones y billones y trillones en la más diminuta mota que puedas ver. Los sólidos, los líquidos, los gases -toda la materia- están hechos de átomos (u otras cosas, como las moléculas, que están hechas de átomos).
 Los ELEMENTOS son los tipos de átomos que podemos tener. El carbono es un elemento, el hidrógeno es un elemento y el oxígeno también. (Podemos llamarlos por sus nombres o por sus símbolos: C para el carbono, H para el hidrógeno y O para el oxígeno). Todos los elementos están recogidos en una tabla periódica. Si está en la tabla, es un elemento.
Los ELEMENTOS son los tipos de átomos que podemos tener. El carbono es un elemento, el hidrógeno es un elemento y el oxígeno también. (Podemos llamarlos por sus nombres o por sus símbolos: C para el carbono, H para el hidrógeno y O para el oxígeno). Todos los elementos están recogidos en una tabla periódica. Si está en la tabla, es un elemento.
Los átomos pueden unirse -forman enlaces- para formar MOLÉCULAS. Por ejemplo, dos átomos de hidrógeno se enganchan para formar una molécula de hidrógeno, H2 para abreviar. Bastante sencillo, ¿no?
Por ejemplo, dos átomos de hidrógeno se enganchan para formar una molécula de hidrógeno, H2 para abreviar. Bastante sencillo, ¿no?
Haz clic aquí para echar un vistazo a un modelo tridimensional de hidrógeno (H2).
Ahora, si metes un átomo de oxígeno entre esos dos hidrógenos, tienes una molécula de agua – ¡H2O!
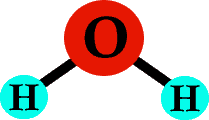
Haz clic aquí para ver el agua (H2O) en 3-D.
Cada tipo de átomo suele formar el mismo número de enlaces (tienden a ser tercos de esa manera). Por ejemplo, un átomo de hidrógeno forma un enlace, un átomo de oxígeno forma dos, y el carbono forma cuatro enlaces. Mira de nuevo esa molécula de agua: cada hidrógeno tiene un enlace, y el oxígeno del centro tiene dos enlaces.
Las moléculas pueden ser mucho más grandes. Una molécula de vitamina C está formada por 20 átomos (6 carbonos, 8 hidrógenos y 6 oxígenos, es decir, C6H8O6). Si tomas esos 20 átomos de vitamina C y los mezclas, uniéndolos en un orden diferente, tendrás una molécula totalmente distinta que no sólo tiene un aspecto diferente, sino que actúa de forma diferente. (¡Si tus piernas salieran de tu cabeza, también actuarías raro!)
| Vitamina C C6H8O6 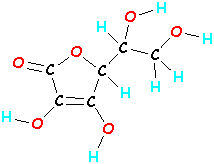 |
Algo más C6H8O6 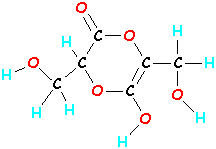 |
Entonces, las moléculas son átomos unidos, pero no de cualquier manera. Cambiar qué átomo está unido a cuál puede cambiar las propiedades de una molécula, es decir, su aspecto y su forma de actuar, y eso cambia el aspecto y la forma de actuar de todo un MONTÓN de moléculas colgadas juntas. Por ejemplo, el agua es un líquido, el hidrógeno es un gas y la vitamina C es un sólido.
«¡¿Y QUÉ?!», te preguntarás. Bueno, cuando hablamos de polímeros, la forma en que los átomos están unidos entre sí puede tener un impacto ENORME en cómo se siente y reacciona algo hecho de esos polímeros cuando lo golpeas o lo pisas o lo tiras contra la pared. Por ejemplo, ¿se pegará a la pared o rebotará?
Una experiencia de enlace
El tipo de enlace del que hemos hablado aquí se llama «enlace covalente», lo que significa que se hace compartiendo electrones entre dos átomos.
Más información sobre el enlace y la estructura de los átomos aquí, si no ….
¡Hablemos de POLÍMEROS!
 |
Volver a los fundamentos de los polímeros |
 |
Volver a la página principal |