
定義
2つの異なる金属や合金が腐食性の溶液に浸されたり、水分によって定期的に接続されたりすると、それぞれに腐食電位が発生します。 ガルバニック腐食の条件が揃っていれば、より高貴な金属が陰極となり、より活発な金属が陽極となります。 陽極と陰極の間には、測定可能な電流が流れることがある。 これが起こると、使用環境における陽極の腐食速度が増加し、陰極の腐食速度は減少します。
ガルバニック腐食は、材料の寿命を延ばすために使用されることがありますが(炭素鋼の亜鉛コーティングや給湯器の亜鉛アノードなど)、考慮されておらず、適切な条件が存在しない場合は、予期しない故障につながる可能性があります。
ガルバニック腐食の条件:
ガルバニック腐食が発生するためには、3つの要素が必要です。
- 異なる腐食電位を持つ2つの金属
- 金属と金属の直接の電気的接触
- 導電性の電解質溶液(例えば水)が定期的に2つの金属を接続する必要があります。 電解質溶液は「導電性の道」を作ります。 これは、定期的な浸漬、結露、雨、霧の暴露など、2つの金属を湿らせて接続する水分源がある場合に発生する可能性があります。
これらの要素のいずれかが欠けていると、ガルバニック・コロージョンは発生しません。
これらの要素のいずれかが欠けていると、電解腐食は起こりません。例えば、2つの金属間の直接の接触が妨げられている場合(プラスチックワッシャー、塗膜など)や、導電経路に何らかの障害がある場合は、電解腐食は起こらず、それぞれの金属はそのサービス環境での通常の速度で腐食します。 図1は、電解腐食の要件をすべて満たさない状態の例を示しています。
図1
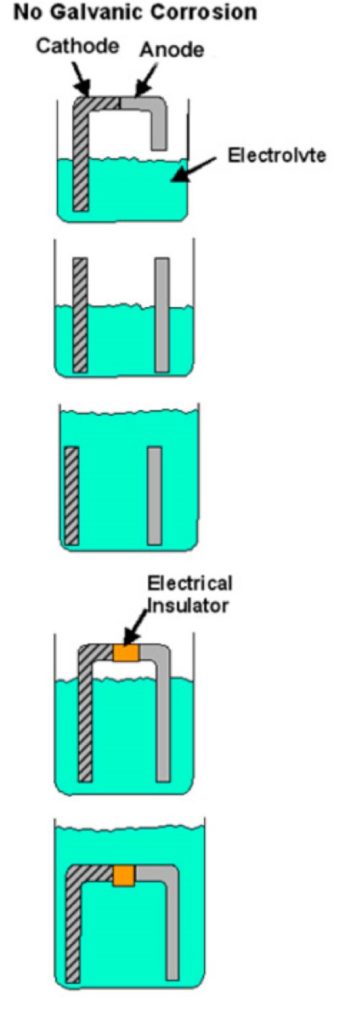
ガルバニック腐食が起こらないバイメタルの組み合わせ例
2つの異なる金属が大気中や水中で結合した場合、ガルバニック腐食が起こる可能性を「ガルバニックシリーズ」で予測することができます。”
図2
図2は、いくつかの一般的な金属や合金について、海水中で測定したガルバニックシリーズです。 2つの金属がリストの中で離れている(例えば、2つの数字の差が大きい)と、ガルバニック腐食の駆動力が大きくなります。 最もアノード性(活性)の高い金属が上に、最もカソード性(貴)の高い金属が下にある。 ステンレス鋼については、実線と中空の両方の棒が示されている。 中空の棒は、積極的に腐食するステンレス鋼を表しており、これは受動的な(腐食しない)ステンレス鋼とは異なる電位を持っています。
例えば、活動的な材料である亜鉛(亜鉛メッキ鋼板を想像してください)がリストの一番上にあり、貴金属であるステンレス鋼がリストの一番下にある場合、電解質(水)の存在下で直接接触すると、定期的に電解質にさらされていれば電解腐食が起こります。

。