Authored by Charles Coffey, MD & Tamer Ghanem, MD PhD; geredigeerd door Ellie Maghami, MD FACS
AHNS Onderwijscommissie
Inleiding
Dit document is bedoeld om een subtype van hoofd-halskanker, bekend als orofarynxkanker, te introduceren en de normale anatomie en fysiologie van de orofarynx zullen de revue passeren. Factoren die kunnen leiden tot het ontstaan van kanker in dit gebied worden gedefinieerd. Informatie over diagnose, behandeling en verwachte resultaten van deze aandoening wordt gegeven.
Anatomie & Functionele overwegingen
De orofarynx is het middelste compartiment van de keelholte, d.w.z. de keel; het is het gebied van de keel tussen de nasopharynx (bovenste compartiment) en de hypopharynx (onderste compartiment). De oropharynx omvat de tonsillen, de tongbasis, het zachte gehemelte en de faryngeale wanden. Verscheidene van deze subregio’s zijn veel voorkomende plaatsen voor de ontwikkeling van hoofd-halskanker, en een tumor in een van deze subregio’s kan in grote lijnen worden gecategoriseerd als een oropharyngeale tumor. Het is belangrijk een onderscheid te maken tussen de orofarynx en de mondholte (mond), omdat tumoren die op deze twee plaatsen ontstaan zich verschillend kunnen gedragen en heel andere overwegingen vereisen wat betreft functie en passende behandeling.
De tonsillen (ook wel palatine tonsillen genoemd) zijn verzamelingen lymfoïd weefsel die zich aan weerszijden van de orofarynx bevinden en een rol spelen in de immuunfunctie van het aerodigestieve systeem. Hoewel de amandelen tijdens de kinderjaren vrij groot kunnen zijn, nemen ze over het algemeen af naarmate men ouder wordt en bij veel volwassenen blijft er maar weinig zichtbaar amandelweefsel over. Vergroting of asymmetrie van de tonsillen bij volwassenen kan gewoon een anatomische variant zijn, maar kan ook wijzen op de aanwezigheid van een tumor. Verwijdering van amandelen heeft de immuunstatus niet aangetast.
De tongbasis (of tongbasis) is het deel van de tong dat zich in de oropharynx (achterste 1/3 van de tong) bevindt. De tongbasis is functioneel en anatomisch te onderscheiden van de mondtong, het deel van de tong dat in de mondholte ligt (voorste 2/3 van de tong) en het belangrijkst is voor spraak en taal. De spieren van de tongbasis zijn meer betrokken bij het slikken dan bij het spreken, en spelen een cruciale rol bij het regelen van de doorgang van voedsel en vloeistoffen van de mond naar de keel. Disfunctie van de tongbasis als gevolg van een tumor, weefselverlies bij een operatie of bestraling kan slikproblemen of aspiratie (het morsen van vloeistoffen in het strottenhoofd of de stemholte) tot gevolg hebben.
Het zachte gehemelte is een gespierde sliert van zacht weefsel die zich achter het harde gehemelte, oftewel het dak van de mond, bevindt. Het zachte gehemelte scheidt de neus en neus-keelholte van de rest van de keelholte en mondholte tijdens het spreken en slikken. Het onvermogen om het zachte gehemelte te sluiten (velopharyngeale insufficiëntie) als gevolg van een tumor, resectie of litteken kan resulteren in hypernasale spraak en het terugvloeien van vloeistoffen in de neus tijdens het slikken. De laterale en posterieure wanden van de oropharynx bestaan voornamelijk uit spieren die een ondersteunende rol spelen in de faryngeale fase van het slikken.
Epidemiologie
De oropharynx is een van de meest voorkomende plaatsen van hoofd- en halskanker in de Verenigde Staten. Naar schatting worden in de Verenigde Staten jaarlijks 11.000-13.000 nieuwe gevallen van orofaryngeale kanker gediagnosticeerd (Jemal; Siegel; CDC). De grote meerderheid van deze tumoren zijn plaveiselcelcarcinomen, een vorm van kanker die ontstaat uit plaveiselepitheelcellen die de bovenste luchtwegen bekleden. Plaveiselcelcarcinomen kunnen ook op tal van andere plaatsen ontstaan, zoals de huid, de longen, de blaas en de baarmoederhals, maar het gedrag van de tumor en de behandelingsmogelijkheden verschillen sterk per lichaamsdeel. Mannen hebben meer dan vier keer zoveel kans als vrouwen om orofaryngeaal plaveiselcelcarcinoom (OPSCC) te ontwikkelen, met een algemeen jaarlijks risico van 6,2 per 100.000 mannen vergeleken met 1,4 gevallen per 100.000 vrouwen (Jemal, CDC). De incidentie in de VS is het hoogst onder blanke en zwarte mannen, en lager onder Hispanics, Native Americans en Asians/ Pacific Islanders.
Risicofactoren
Tabak en Alcohol
Tabakgebruik is duidelijk vastgesteld als de primaire risicofactor voor de meerderheid van de hoofd-halskankers van het spijsverteringskanaal (Sturgis 04, Sturgis 07). Het levenslange risico op het ontwikkelen van hoofd-halskanker is 10-voudig verhoogd bij rokers, en de omvang van het risico neemt tot 25-voudig toe bij de zwaarste rokers. Alcoholgebruik is een onafhankelijke risicofactor voor de ontwikkeling van hoofd-halskanker. Hoewel het risico groter is bij chronisch zwaar alcoholgebruik, zijn er aanwijzingen dat licht alcoholgebruik ook het risico op het ontwikkelen van orofaryngeale kanker kan verhogen (Bagnardi). Gecombineerd gebruik van zowel tabak als alcohol verhoogt het risico op kanker nog meer (Masberg). Historisch wordt tot 90% van de squameuze celcarcinomen in hoofd en nek, waaronder OPSCC, toegeschreven aan tabaksgebruik en alcoholmisbruik (Sturgis 04). Het tabaksgebruik in de Verenigde Staten is de laatste vijf decennia gestaag gedaald, waarbij het percentage actieve rokers is gedaald van 43% in 1965 tot minder dan 20% in 2010 (Mariolis, Skinner). Het alcoholgebruik per hoofd van de bevolking vertoont een bescheidener daling, van 2,7 gallon per jaar in het midden van de jaren tachtig tot 2,26 gallon per jaar in 2010 (LaVallee). Deze trends zijn over het algemeen parallel verlopen met dalende percentages van hoofd-halskankerincidentie en -sterfte.
Human Papilloma Virus
Ondanks de dalende percentages van tabaks- en alcoholgebruik, vertonen de percentages van orofaryngeale kanker de laatste tien jaar een gestage opwaartse trend. Dit is voornamelijk te wijten aan de toename van kankers die verband houden met infectie met het humaan papilloma virus (HPV). Humane papilloma-virussen zijn een grote groep verwante virussen die worden verspreid via vaginale, orale en anale seks. HPV is de meest voorkomende seksueel overdraagbare infectie in de Verenigde Staten en treft meer dan de helft van de seksueel actieve personen op een bepaald moment in hun leven (NCI). Verschillende stammen van HPV worden in verband gebracht met een verhoogd risico op het ontwikkelen van baarmoederhals-, genitale en orofaryngeale kanker. Infectie van epitheelcellen door hoogrisicostammen van HPV gaat gepaard met de productie van virale eiwitten die uiteindelijk het normale vermogen van de cel om tumorgroei te onderdrukken, kunnen verstoren. Het immuunsysteem slaagt erin HPV-infectie bij de meeste patiënten te elimineren en slechts een klein deel van de patiënten die geïnfecteerd zijn met hoog-risico HPV-stammen zal een HPV-gerelateerde vorm van kanker ontwikkelen. Naar schatting heeft ongeveer 7% van de mensen in de leeftijd van 14 tot 69 jaar in de VS op enig moment een orale HPV-infectie, zoals gedetecteerd door een mondspoeling. Ongeveer de helft (3,7%) van deze infecties is met hoog-risico HPV-stammen (Gillison 2012; Sanders). Het tijdsverloop tussen een orale HPV-infectie en de ontwikkeling van HPV-gerelateerde orofaryngeale kanker wordt geschat op 15 tot 30 jaar. Als zodanig weerspiegelt de toename van OPSCC sinds de jaren 1990 voor een groot deel veranderingen in seksuele praktijken in de jaren 1960 en 1970.
Het risicoprofiel voor HPV-gerelateerde OPSCC verschilt van de meeste hoofd-halskankers. In vergelijking met patiënten met niet-HPV-tumoren zijn patiënten met HPV-positief OPSCC vaker jong, blank, hebben een hogere sociaaleconomische status, roken niet en drinken niet. Seksuele voorgeschiedenis is sterk geassocieerd met HPV-positieve kankers. Een significante toename van het risico op OPSCC is in verband gebracht met het aantal seksuele partners tijdens het leven, orale seks, vroegere leeftijd bij seksueel debuut, onregelmatig gebruik van barrièremiddelen tijdens seks, een levenslange geschiedenis van seksueel overdraagbare aandoeningen, en, bij mannen, met een geschiedenis van seksueel contact tussen personen van hetzelfde geslacht (Heck; Gillison 2008).
Er is een verband aangetoond tussen hoofd-halskanker en marihuanagebruik, maar het blijft onzeker of marihuanagebruik een onafhankelijke risicofactor is voor OPSCC (Gillison 2008). Slechte mondgezondheid, inclusief parodontale aandoeningen en tandverlies, is betrokken bij de etiologie van oraal en orofaryngeaal carcinoom, maar de associaties zijn bescheiden en het bewijs is over het algemeen niet overtuigend (Divaris). Een hoge inname van fruit en groenten via de voeding kan enigszins beschermend zijn voor mond- en keelholtekanker, hoewel het bewijs hiervoor niet overtuigend is (Lucenteforte).
Diagnose & Evaluatie
Een patiënt met een hardnekkige massa in de hals of keel of met symptomen die wijzen op orofarygneale kanker moet worden doorverwezen naar een otolaryngoloog (KNO-arts) of hoofd-hals chirurg voor verdere evaluatie. Symptomen van orofarynxkanker kunnen zijn: pijn in de keel, slikproblemen, gewichtsverlies, oorpijn, stemverandering en speeksel met een bloedige smaak. De eerste evaluatie bestaat uit een gedetailleerde anamnese en een uitgebreid onderzoek van het hoofd en de nek, meestal inclusief onderzoek van de keelholte en het strottenhoofd met een kleine flexibele endoscoop, uitgevoerd in een kantooromgeving. Bij verdachte tumoren van de oropharynx moet een biopsie worden genomen voor histopathologisch onderzoek. In vele gevallen is het mogelijk een biopsie in de kliniek te verrichten indien een laesie gemakkelijk toegankelijk is, hetzij rechtstreeks via de mond, hetzij via een flexibele endoscopie. In veel gevallen vereist de evaluatie echter aanvullend onderzoek en biopsie onder algehele anesthesie in een operatiekamer. Dergelijke procedures kunnen over het algemeen in minder dan dertig minuten worden voltooid en kunnen in de meeste gevallen poliklinisch worden uitgevoerd. In bepaalde omstandigheden is het mogelijk om via een naaldbiopsie (fijne naaldaspiratie, of FNA) voldoende weefsel voor de diagnose te verkrijgen indien een lymfeklier in de hals door kanker is aangetast (d.w.z. een nodale metastase). Naaldbiopsie wordt meestal in de kliniek uitgevoerd en vereist geen verdoving, hoewel het niet dezelfde informatie over het stadium kan opleveren als onderzoek onder verdoving. Testen van biopsiestalen op HPV-status wordt in alle gevallen aanbevolen. HPV-positieve status voorspelt betere resultaten met standaardtherapieën in het algemeen, maar deze informatie mag momenteel niet worden gebruikt om beslissingen over behandeling af te stemmen, met uitzondering van zorgvuldig gecontroleerde klinische trials.
Alle patiënten met een bevestigde diagnose van OPSCC moeten worden geëvalueerd door een multidisciplinair behandelingsteam. Beeldvorming moet worden verkregen om de primaire tumor, de betrokkenheid van lymfeklieren in de hals, en voor aanwijzingen van uitgezaaide kanker buiten het hoofd en de hals te evalueren. Zorgverleners kunnen kiezen voor computertomografie (CT-scan) of magnetische resonantiebeeldvorming (MRI) van de hals om de keelholte en de lymfeklieren in de hals te beoordelen. Deze scan moet in bijna alle gevallen worden uitgevoerd met IV-contrast, met uitzondering van patiënten met een verminderde nierfunctie of een allergie voor contrastmiddel. Een CT-scan van de borstkas is in de meeste gevallen ook geïndiceerd om na te gaan of er uitgezaaide kanker in de longen of de lymfeklieren van de borstkas aanwezig is. Positronemissietomografie (PET-scan) wordt ook steeds vaker gebruikt voor de evaluatie van de voorbehandeling, met name bij patiënten met een gevorderd ziektestadium.
Als onderdeel van de evaluatie van de voorbehandeling moeten alle patiënten die kiezen voor bestralingstherapie vóór de behandeling een tandheelkundige evaluatie ondergaan. Als gevolg van de effecten van bestraling op bot en omliggend weefsel is er een aanzienlijk verhoogd risico op botgerelateerde complicaties bij tandheelkundige ingrepen die na bestraling worden uitgevoerd. In de ernstigste gevallen kan extractie van het gebit of infectie na bestraling leiden tot afsterven van het botweefsel (osteoradionecrose), waardoor operatieve verwijdering van het bot noodzakelijk wordt. Om het risico op deze complicaties zo klein mogelijk te houden, kan worden aangeraden de tanden vóór de bestraling te trekken als er aanwijzingen zijn voor tandbederf of een vergevorderde parodontale aandoening. Alle patiënten moeten vóór de behandeling worden onderworpen aan een voedings-, spraak- en sliktest. Patiënten die aanzienlijk gewichtsverlies of slikproblemen ondervinden als gevolg van OPSCC kunnen baat hebben bij het operatief plaatsen van een voedingssonde in de maag voorafgaand aan de behandeling. Veel patiënten zijn echter in staat om tijdens de gehele behandeling oraal te blijven eten, en het plaatsen van een voedingssonde is niet voor alle patiënten noodzakelijk. Indien mogelijk moeten patiënten die een behandeling voor OPSCC ondergaan, tijdens de behandeling via de mond blijven eten en drinken, zolang dit door het behandelteam als veilig wordt beschouwd. Oefening van de farynxspieren tijdens de behandeling kan helpen om een normale slikfunctie te behouden, zowel tijdens als na de kankertherapie.
Bij een kleine subset van patiënten wordt plaveiselcelkanker alleen gediagnosticeerd door middel van een naaldaspiratiebiopsie van een abnormaal vergrote lymfeklier. In deze gevallen is het mogelijk dat bij lichamelijk onderzoek, beeldvorming en intraoperatieve biopsie geen duidelijke kanker in de keel wordt gevonden. Deze gevallen worden “onbekende primaire kanker” genoemd omdat de plaats waar de primaire kanker zich ontwikkelt verborgen blijft. In deze gevallen is het bijzonder aan te bevelen het naaldaspiraat te testen op HPV. Een HPV-positieve status wijst erop dat de orofarynx de meest waarschijnlijke plaats is waar de kanker is ontstaan en voorspelt een beter resultaat.
Stagering
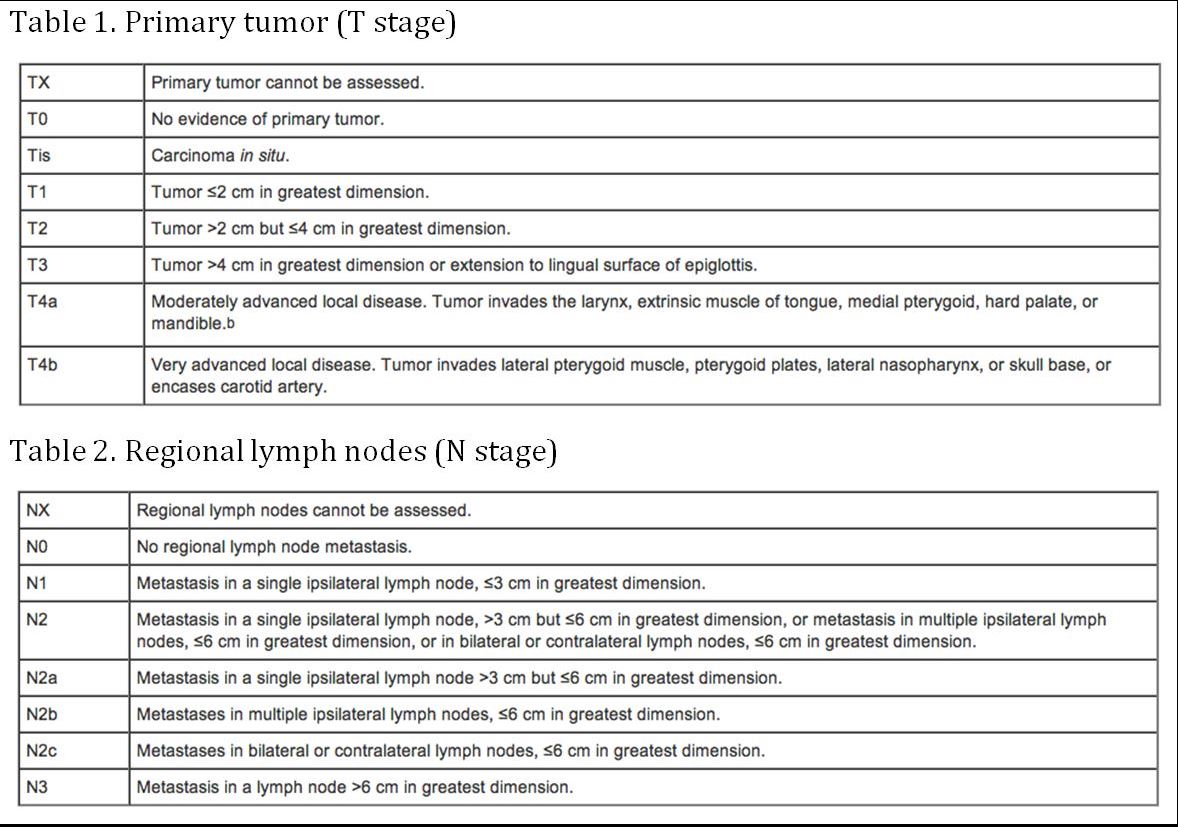

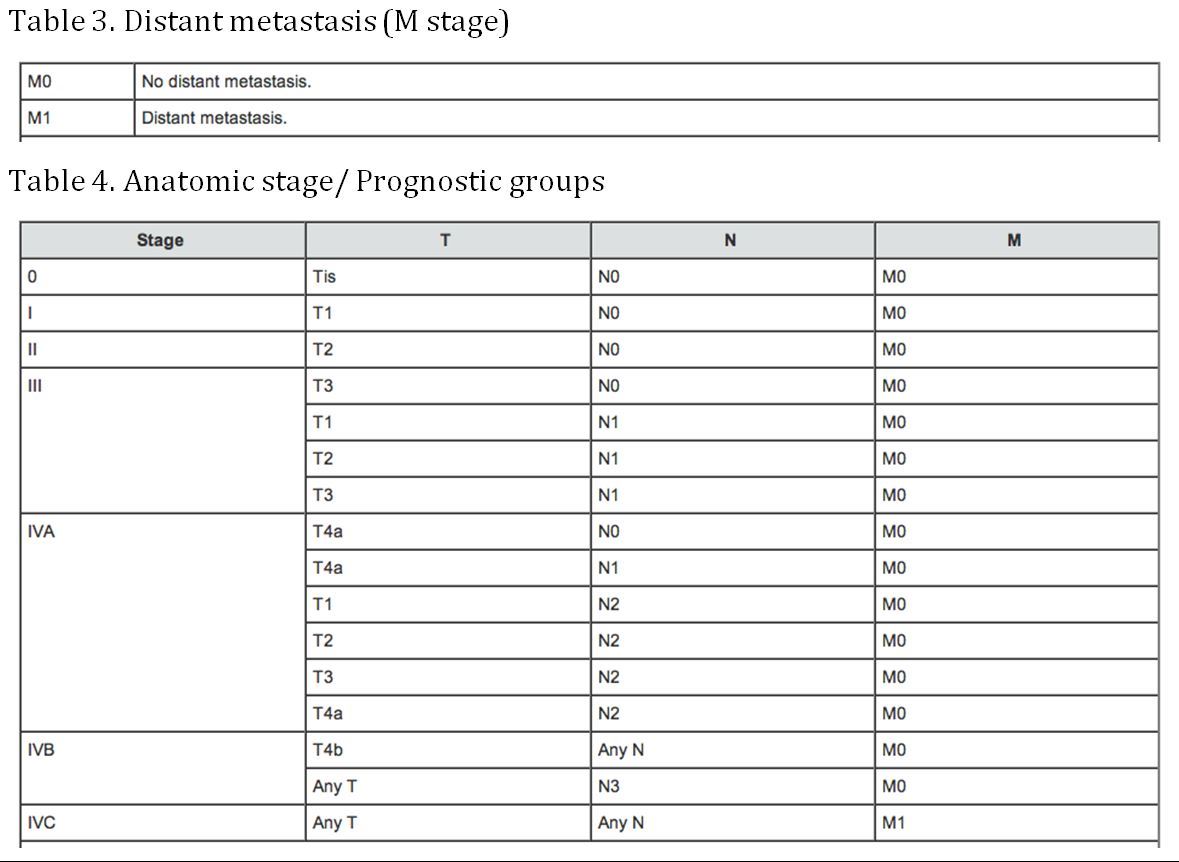

(AJCC: Farynx. In: Edge SB, Byrd DR, Compton CC, et al., eds: AJCC Cancer Staging Manual. 7e ed. New York, NY: Springer, 2010, pp 41-56)