
OK, dus — wat is een atoom en wat heeft het met moleculen te maken?
Laten we het over piepklein hebben, en dan bedoel ik ook echt piepklein. ATOOMEN zijn de basisbouwstenen van alles wat je om je heen kunt zien, en zelfs van veel dingen die je niet kunt zien, zoals de lucht die je inademt. Atomen zijn zo klein dat er miljoenen en miljarden en triljoenen zijn in het kleinste vlekje dat je kunt zien. Vaste stoffen, vloeistoffen, gassen – alle materie – bestaat uit atomen (of andere dingen, zoals moleculen, die van atomen zijn gemaakt)!
 ELEMENTEN zijn de soorten atomen die we kunnen hebben. Koolstof is een element, waterstof is een element, en zuurstof ook. (We kunnen ze bij hun naam noemen, of bij hun symbool – C voor koolstof, H voor waterstof, en O voor zuurstof). Alle elementen staan opgesomd in een periodiek systeem. Als het in de tabel staat, is het een element!
ELEMENTEN zijn de soorten atomen die we kunnen hebben. Koolstof is een element, waterstof is een element, en zuurstof ook. (We kunnen ze bij hun naam noemen, of bij hun symbool – C voor koolstof, H voor waterstof, en O voor zuurstof). Alle elementen staan opgesomd in een periodiek systeem. Als het in de tabel staat, is het een element!
Atomen kunnen aan elkaar haken – ze vormen samen bindingen – om MOLECULEEN te maken. Bijvoorbeeld, twee atomen waterstof haken aan elkaar om een molecuul waterstof te vormen, afgekort H2. Heel eenvoudig, hè?
Bijvoorbeeld, twee atomen waterstof haken aan elkaar om een molecuul waterstof te vormen, afgekort H2. Heel eenvoudig, hè?
Klik hier om een 3-D model van waterstof (H2) te bekijken.
Als je nu een zuurstofatoom tussen die twee waterstofatomen plaatst, heb je een watermolecuul – H2O!
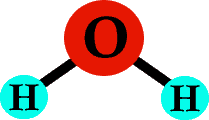
Klik hier om water (H2O) in 3-D te zien.
Elk type atoom vormt meestal hetzelfde aantal bindingen (zo zijn ze meestal koppig). Zo vormt een waterstofatoom één binding, een zuurstofatoom twee, en koolstof vier. Kijk nog eens naar dat watermolecuul – elk waterstofatoom heeft één binding, en de zuurstof in het midden heeft twee bindingen.
Moleculen kunnen veel groter zijn. Een molecuul vitamine C bestaat uit 20 atomen (6 koolwaterstoffen, 8 waterstofatomen en 6 zuurstofatomen – dat is C6H8O6). Als je die 20 atomen vitamine C door elkaar husselt en in een andere volgorde aan elkaar bindt, krijg je een totaal andere molecule die er niet alleen anders uitziet, maar ook anders werkt. (Als je benen uit je hoofd zouden steken, zou je je ook vreemd gedragen!!)
| Vitamine C C6H8O6 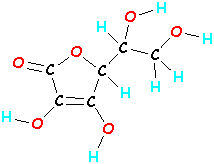 |
Somebody Else C6H8O6 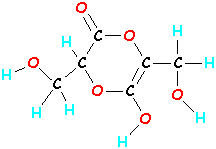 |
Dus, moleculen zijn atomen die aan elkaar vastzitten, maar niet zomaar. Door te veranderen welk atoom aan welk atoom is vastgeplakt, kunnen de eigenschappen van een molecuul veranderen, dat wil zeggen hoe het eruit ziet en zich gedraagt – en dat verandert hoe een hele BONK moleculen die aan elkaar hangen eruit zullen zien en zich zullen gedragen. Water is bijvoorbeeld een vloeistof, waterstof is een gas, en vitamine C is een vaste stof.
“ZO WAT?!!” vraag je je af. Nou, als we het over polymeren hebben, dan kan de manier waarop de atomen aan elkaar zijn gebonden een HUGE invloed hebben op hoe iets dat van die polymeren is gemaakt, aanvoelt en reageert als je erop slaat, erop stapt of het tegen de muur gooit. Blijft het aan de muur kleven of stuitert het weg?
Een bindingservaring
Het soort binding waar we het hier over hebben, heet een “covalente binding”, wat betekent dat die tot stand komt door elektronen tussen twee atomen te delen.
Meer over bindingen en de structuur van atomen hier, anders ….
Let’s talk POLYMERS !!!
 |
Terug naar Polymeer Basis |
 |
Terug naar hoofdpagina |