Doelstellingen
- Begrijp de huidige beperkingen van het vermogen van artsen om prognoses te geven.
- Lijst de variabelen die kunnen worden gebruikt om behandelingsbeslissingen en prognose bij oudere patiënten te sturen.
- Begrijp de cognitieve stappen om prognose bij oudere patiënten te bepalen.
Case & Commentaar: Deel 1
Een 91-jarige vrouw presenteerde zich met 2 dagen van misselijkheid en braken. Lichamelijk onderzoek toonde een palpabele massa in de rechter lies zonder darmgeluiden. Een CT-scan van het abdomen toonde een geïncarneerde hernia gecompliceerd met een kleine darmobstructie. De patiënte werd naar de operatiekamer gebracht voor resectie onder algehele anesthesie. Na extubatie ontwikkelde ze stridor, waardoor re-intubatie nodig was. Uit een KNO-onderzoek bleek dat er geen aanwijzingen waren voor larynxoedeem; er waren echter wel aanwijzingen voor aanzienlijke extrinsieke compressie van de trachea. Een CT-scan toonde een schildkliermassa. Een fijne naald aspiratie (FNA) biopsie werd uitgevoerd, maar was niet doorslaggevend. Er werd een herhaalde FNA verricht.
De behandelend arts hield een familiebijeenkomst om de prognose van de patiënt en de richting van de zorg te bespreken. Hij vertelde de familie dat de prognose waarschijnlijk zeer slecht was, omdat hij maligniteit vermoedde. Gezien dit nieuws besloot de familie af te zien van een chirurgische ingreep (tracheostomie).
Chirurgen worden vaak gevraagd voorspellingen te doen over de verwachte overleving van de patiënt en deze voorspellingen aan de patiënt mee te delen. Onderzoek heeft ook aangetoond dat beide soorten prognostische taken extreem moeilijk zijn voor artsen.
Resultaten van een enquête onder een willekeurige steekproef van 1.311 Amerikaanse internisten suggereren dat de gemiddelde internist de vraag “Hoe lang heb ik nog te leven?” tien keer per jaar stelt, vijf keer per jaar life support intrekt, en vijf keer per jaar patiënten doorverwijst naar palliatieve zorg in een hospice.(1) Van deze artsen gaf 60% aan dat ze prognosticeren emotioneel “stressvol” vonden, en hun stress met prognosticeren was sterk geassocieerd met zelf waargenomen prognostische onnauwkeurigheid.
Data over de prognostische nauwkeurigheid van artsen zijn voornamelijk afkomstig uit studies van artsen die zorgen voor patiënten die al in de palliatieve zorg zijn opgenomen. Uit deze studies blijkt dat artsen gemiddeld onnauwkeurige prognostische schattingen maken; de richting van hun fout is overwegend optimistisch, waarbij artsen de overleving met een factor drie overschatten.(2-8) In één studie gaven 343 artsen schattingen van de overleving voor 468 terminaal zieke kanker- en niet-kankerpatiënten op het moment dat de patiënt werd doorverwezen naar palliatieve zorg in een hospice. Deze schattingen werden vervolgens vergeleken met de daadwerkelijke overleving van de patiënten. Artsen waren in ongeveer 20% van de gevallen accuraat in hun prognoses, overschatten de overleving meer dan drie keer zo vaak (63%), en onderschatten de overleving slechts in een minderheid van de gevallen (17%).(8)
Onderzoek heeft de vraag gesteld of deze systematische overschatting van de prognose door artsen een deel van de verklaring kan zijn voor de onverwacht “korte” overlevingskansen die worden waargenomen bij patiënten die zijn doorverwezen voor palliatieve zorg in een hospice. De resultaten van bovengenoemd onderzoek suggereren dat artsen denken dat een optimale verblijfsduur in een hospice 3 maanden is (9), terwijl de waargenomen mediane verblijfsduur slechts 3 weken is.(8) Misschien is een deel van deze waargenomen inconsistentie het gevolg van de optimistische vooringenomenheid van artsen bij het voorspellen van de prognose.
Deze patiënt verschilde van de patiënten die deelnamen aan bovengenoemde onderzoeken, omdat er bij haar nog geen “terminale ziekte” was vastgesteld. Aangezien de wetenschap van de prognose is verankerd in de diagnose en de omvang van de ziekte, droeg de diagnostische dubbelzinnigheid van deze patiënte ertoe bij dat de prognose een grote uitdaging werd. Aan de ene kant, als de nekmassa van de patiënte het resultaat was van anaplastische schildklierkanker (d.w.z. een zeldzame en snel dodelijke vorm van schildklierkanker), zou haar geschatte mediane overleving ongeveer 4 maanden bedragen (10), en zou de onmiddellijke instelling van ondersteunende (en niet-curatieve) zorg een passende klinische benadering zijn om de luchtwegcompromis te beheersen. Aan de andere kant, als haar nekmassa het resultaat was van een goedaardige struma, zou haar geschatte mediane overleving waarschijnlijk vergelijkbaar zijn met haar leeftijdsgerelateerde verwachte basisoverleving van ongeveer 4 jaar (11), en zou het instellen van ondersteunende zorg geen conventionele benadering zijn van het beheer van de luchtwegcompromis. Afhankelijk van de kenmerken van de struma (bijv. diffuus, multinodulair) en de aanpak van de endocrinoloog (bijv. T4-onderdrukkende therapie, reductieve chirurgie en/of radioactief jodium), zouden andere benaderingen meer conventioneel zijn.
Gezien het zeer brede prognostische bereik dat geassocieerd wordt met de halsmassa van deze patiënte – 4 maanden versus 4 jaar – en het bijbehorende brede scala aan klinische benaderingen, zou een weefseldiagnose voor deze patiënte helpen om dit prognostische bereik te verkleinen en zo de onmiddellijke klinische aanpak beter te definiëren. Hoewel een clinicus geneigd zou kunnen zijn om aan te nemen dat een grote massa kanker is, suggereren studies van opeenvolgende schildklieraspiraties in openbare ziekenhuizen dat kanker slechts 5% tot 6,5% (12,13) van de knobbels verklaart.
Case & Commentaar: Deel 2
Na verdere discussie besloot de familie de zorg af te bouwen, omdat patiënte eerder had verklaard dat zij niet langdurig geïntubeerd wilde worden. Kort na de extubatie overleed de patiënte. Een paar dagen na het overlijden van de patiënte werden de resultaten van de tweede FNA verkregen. De biopsie toonde een goedaardige nodulaire struma.
De patiënt, de familie en de arts in dit vignet beleefden de ongewone situatie van een pessimistische prognostische fout. De beschreven gebeurtenissen zijn verrassend en roepen een belangrijke vraag op: waarom werd de FNA gedaan als de resultaten de zorg niet zouden beïnvloeden?
Een natuurlijk punt van zorg in dit geval is of de hoge leeftijd van de patiënt op de een of andere manier van invloed is geweest op de beslissing om een minder volledige diagnostische benadering te volgen. Het is zeker moeilijk voor te stellen dat een 37-jarige vrouw op deze manier zou zijn behandeld. Het is echter mogelijk dat er andere levensbedreigende comorbiditeiten waren (bv. een eerder gediagnosticeerde kanker in een gevorderd stadium, ernstige dementie, klasse IV congestief hartfalen) en/of een slechte functionele status die haar onderliggende of uitgangsprognose beïnvloedden en aldus de klinische benadering zouden kunnen verklaren.
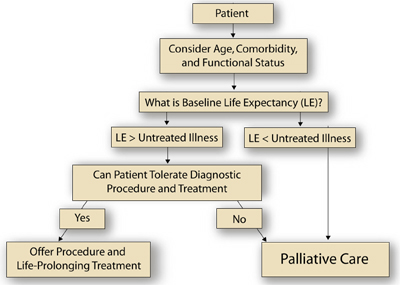
Een algemene klinische benadering van deze patiënte kan worden ontleend aan de oncologie, die momenteel worstelt met het ontwikkelen van systematische benaderingen of algoritmen die belangrijke prognostische variabelen (zowel kankergerelateerd als niet-kankergerelateerd) erkennen en integreren om beslissingen over de behandeling van kanker bij oudere patiënten te sturen.(14) Een uitgebreide geriatrische evaluatie (CGA) kan bijvoorbeeld informatie opleveren over functionele status en comorbiditeiten, die samen met geslacht en chronologische leeftijd prognostisch relevant zijn en kunnen worden geïntegreerd om een schatting van de basislevensverwachting te genereren.(14) De arts vergelijkt de verwachte overleving van de onbehandelde ziekte of ziekten die worden overwogen (bv. anaplastische schildklierkanker vs. goedaardige goiter) met deze schatting van de basislevensverwachting. Als de basislevensverwachting groter is dan die van de onbehandelde aandoening, moet de arts vervolgens beslissen of de diagnostische procedure en/of de ziektespecifieke behandeling zou resulteren in overmatige morbiditeit en mortaliteit (d.w.z. beslissen of de interventies “verdraagbaar” zijn). Als de diagnostische procedure en/of de behandelingstolerantie voldoende wordt geacht, dan kan de patiënt baat hebben bij verder onderzoek en, uiteindelijk, therapie gericht op de ziekte of het ziektebeeld in kwestie.
In dit geval wordt geen informatie gegeven over comorbiditeit of functionele status, maar we weten wel dat de patiënt een 91-jarige vrouw was. Levenstabellen geven aan dat 50% van de 90-jarige Amerikaanse vrouwen ten minste nog 3,8 jaar zal leven, waarvan 25% minder dan 1,8 jaar en 25% ten minste 6,8 jaar. Aangezien de verwachte overleving van de meest agressieve schildklierkanker (d.w.z. anaplastische histologie) slechts 4 maanden bedraagt en de verwachte overleving van de meest goedaardige verklaring voor de halsmassa (d.w.z. goedaardige struma) de levensverwachting waarschijnlijk niet noemenswaardig zal beïnvloeden, zouden de meeste algoritmen een biopsie aanbevelen. Indien de patiënt daarentegen reeds een ernstige levensbeperkende ziekte had (bv. longkanker stadium IV), zouden de resultaten van de biopsie geen invloed hebben op de besluitvorming en zou biopsie dus niet nodig zijn. In dit laatste geval zou ondersteunende zorg voor de longkanker een geschikte aanpak zijn. De figuur schetst een benadering van dergelijke klinische besluitvorming voor oudere patiënten met kanker.
Bij het maken van prognostische schattingen bij oudere patiënten is het belangrijk de volgende zaken in overweging te nemen:
- Wat is de diagnose en omvang van de nieuwe ziekte?
- Wat is de basale levensverwachting van de patiënt gerelateerd aan leeftijd, comorbiditeit en functionele status?
- Is de verwachte overleving van de nieuwe ziekte korter dan de basale levensverwachting?
- Zal behandeling de verwachte overleving van de nieuwe ziekte verbeteren?
- Zal behandeling voor de nieuwe ziekte worden verdragen?
Prognosticatie is een moeilijke taak. De meeste artsen zijn niet in staat om de overleving nauwkeurig te voorspellen en voelen zich ongemakkelijk bij het proces. Waar mogelijk moet een op bewijs gebaseerde aanpak worden gevolgd, waarbij het effect van vooroordelen uit het algoritme moet worden verwijderd, maar verder onderzoek is nodig om klinisch bruikbare voorspellende algoritmen te ontwikkelen.(16-20)
Elizabeth B. Lamont, MD, MS Assistant Professor of Medicine Harvard Medical School Massachusetts General Hospital Cancer Center and Institute of Technology Assessment
Faculty Disclosure: Dr. Lamont heeft verklaard dat noch zijzelf, noch een direct familielid van haar, een financiële regeling heeft of een andere relatie heeft met de fabrikanten van commerciële producten die in deze medische nascholingsactiviteit worden besproken. Bovendien bevat haar commentaar geen informatie over onderzoek naar of off-label gebruik van farmaceutische producten of medische hulpmiddelen.
1. Christakis NA, Iwashyna TJ. Attitude and self-reported practice regarding prognostication in a national sample of internists. Arch Intern Med. 1998;158:2389-95.
2. Christakis NA, Lamont EB. Extent and determinants of error in doctors’ prognoses in terminally ill patients: prospective cohort study. BMJ. 2000;320:469-72.
3. Parkes CM. Accuracy of predictions of survival in later stages of cancer. BMJ. 1972;2:29-31.
4. Evans C, McCarthy M. Prognostic uncertainty in terminal care: can the Karnofsky index help? Lancet. 1985;1:1204-6.
5. Heyse-Moore LH, Johnson-Bell VE. Can doctors accurately predict the life expectancy of patients with terminal cancer? Palliat Med. 1987;1:165-6.
6. Forster LE, Lynn J. Predicting life span for applicants to inpatient hospice. Arch Intern Med. 1988;148:2540-3.
7. Maltoni M, Nanni O, Derni S, et al. Klinische voorspelling van overleving is nauwkeuriger dan de Karnofsky performance status bij het schatten van de levensduur van terminaal zieke kankerpatiënten. Eur J Cancer. 1994;30A:764-6.
8. Christakis NA, Lamont EB. Extent and determinants of error in doctors’ prognoses in terminally ill patients: prospective cohort study. BMJ. 2000;320:469-72.
9. Iwashyna TJ, Christakis NA. Attitude and self-reported practice regarding hospice referral in a national sample of internists. J Palliat Med. 1998;1:241-8.
10. Seesions RB, Burman KD. Kanker van de schildklier. In: Harrison LB, Sessions RB, Hong KW, eds. Kanker van hoofd en hals. 2nd ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2004.
11. Walter LC, Covinsky KE. Cancer screening in elderly patients: a framework for individualized decision making. JAMA. 2001;285:2750-6.
12. Belfiore A, Giuffrida D, La Rosa GL, et al. High frequency of cancer in cold thyroid nodules occurring at young age. Acta Endocrinol (Copenh). 1989;121:197-202.
13. Belfiore A, Giuffrida D, La Rosa GL, et al. High frequency of cancer in cold thyroid nodules occurring at young age. Acta Endocrinol (Copenh). 1989;121:197-202.
14. Repetto L, Granetto C, Venturino A, Rosso R, Gianni W, Santi L. Prognostic evaluation of the older cancer patient. In: Balducci L, Lyman GH, and Ershler WB, eds. Comprehensive geriatric oncology. 1e ed. Amsterdam, The Netherlands: Harwood Academic Publishers; 1998:287-300.
15. Balducci L. Hebben we geriatrische oncologie nodig? Kankerbestrijding. 1994;1:91-93.
16. Lamont EB, Christakis NA. Overlevingsschattingen bij gevorderde kanker. In: Rose BD, ed. UpToDate (versies 10.2-10.3). UpToDate. Wellesley, MA; 2002. Beschikbaar op : . Accessed August 17, 2004.
17. Lamont EB, Christakis NA. Prognostication in advanced disease. In: Berger A, Portenoy RK, Weissman DE, eds. Beginselen en praktijk van palliatieve zorg en ondersteunende oncologie. 2nd ed. Philadelphia, PA: Lippincott Williams and Wilkins; 2002.607-14.
18. Fox E, Landrum-McNiff K, Zhong Z, Dawson NV, Wu AW, Lynn J. Evaluation of prognostic criteria for determining hospice eligibility in patients with advanced lung, heart, or liver disease. SUPPORT Onderzoekers. Studie om prognoses en voorkeuren voor uitkomsten en risico’s van behandelingen te begrijpen. JAMA. 1999;282:1638-45.
19. Schonwetter RS, Han B, Small BJ, Martin B, Tope K, Haley WE. Predictors of six-month survival among patients with dementia: an evaluation of hospice Medicare guidelines. Am J Hospiat Care. 2003;20:105-13.
20. Arias E. Verenigde Staten levenstafels, 2000. . 2002;51:29-33. Beschikbaar op: . Accessed August 17, 2004.
Figuur
Figuur. Een algoritme voor de behandeling van oudere kankerpatiënten